Действие - лиганд
Cтраница 3
К практическим применениям указанного общего подхода принадлежит один из квантовохимических методов расчета свойств неорганических комплексных соединений - так называемая теория кристаллического поля, которая основана на следующей модели. Гамильтониан свободного атома, в котором учитываются только электростатические взаимодействия, инвариантен относительно одновременного вращения координат всех электронов. Если атом теперь подвергнется действию лигандов ( химически связанных с ним соседних атомов) и возникший при этом комплекс будет иметь симметрию, отвечающую группе G, то исходная сферическая симметрия атома нарушится и вместе с ней изменится исходное вырождение уровней. Квантовые числа L и ML перестают быть хорошими квантовыми числами, поэтому вместо них следует ввести новые квантовые числа Г и тт, где Г - неприводимое представление группы G, a mr - компонента этого представления, если неприводимое представление Г является многомерным. Следовательно, исходный пятикратно вырожденный уровень расщепляется на два новых энергетических уровня, один из которых трехкратно вырожден, а другой двукратно вырожден. [31]
Из приведенного выше краткого рассмотрения вопроса о влиянии солей на белки ясно, что до конца понять этот вопрос еще не удалось. В настоящее время он активно изучается во многих лабораториях. Наиболее вероятной представляется точка зрения, согласно которой действие лигандов при высаливании белков зависит как от степени их гидратации, так и от их способности непосредственно взаимодействовать с макромолекулами. В обоих случаях наиболее существенны свойства лигандов, присущие им как льюисовским основаниям. Идеи, лежащие в основе теории поля лигандов, могут быть распространены и на тяжелые металлы, хотя расчеты в этом случае могут быть выполнены лишь для элементов с незаполненными rf - орби-талями. [32]
 |
Растворимость тетрафтороборатов щелочных металлов в различных растворителях. [33] |
В тех случаях, когда можно получить безводные соли, их стабильность в значительной степени зависит от радиуса и поляризующей способности катиона. Высокозаряженные катионы малого объема образуют простые фториды с большой энергией решетки; тетрафторобораты этих ионов стабильны только при наличии комплексных катионов. Катион может образовать комплекс, а тетрафтороборат - стабилизироваться при действии незаряженных лигандов, например воды, аммиака, алкильных или арильных групп, или даже отрицательными ионами, например фторид-ионом. [34]
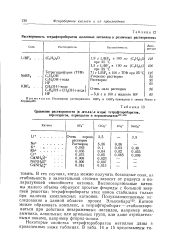 |
Растворимость тетрафтороборатов щелочных металлов в различных растворителях. [35] |
В тех случаях, когда можно получить безводные соли, их стабильность в значительной степени зависит от радиуса и поляризующей способности катиона. Вышкозаряженные катионы малого объема образуют простые фториды с большой энергией решетки; тетрафторобораты этих ионов стабильны только при наличии комплексных катионов. Катион может образовать комплекс, а тетрафтороборат - стабилизироваться при действии незаряженных лигандов, например воды, аммиака, алкильных или арильных групп, или даже отрицательными ионами, например фторид-ионом. [36]
Характеристика распределения зарядов в комплексной частице не исчерпывает вопроса о валентном состоянии центрального иона. В принципе после образования соединения нужно рассматривать не валентные орбитали атома, а возникшие молекулярные орби-тали. Однако ряд допустимых приближений иногда позволяет считать, что атомные орбитали иона металла сохраняются при вхождении его в комплексную частицу, но испытывают возмущение под действием лигандов, в связи с чем может измениться порядок их заполнения электронами. [37]
Характеристика распределения зарядов в комплексной частице не исчерпывает вопроса о валентном состоянии центрального иона. В принципе после образования соединения нужно рассматривать не валентные орбитали атома, а возникшие молекулярные орбитали. Однако ряд допустимых приближений иногда позволяет считать, что атомные орбитали центрального иона металла сохраняются при вхождении его в комплексную частицу, но испытывают возмущение под действием лигандов, в связи с чем может измениться порядок их заполнения электронами. [38]
Для тяжелых металлов характерно стремление к образованию низкоспиновых соединений. Это значит, что в тех состояниях окисления, где элемент имеет нечетное число электронов, чаще всего бывает только один неспаренный электрон; если же электронов четное число, то соединения очень часто диамагнитны. Во-первых, вследствие большей протяженности 4а - и Sd-орби-талей по сравнению с Sd-орбиталями находящаяся на них пара электронов будет испытывать меньшее взаимное отталкивание. Во-вторых, под действием лигандов данного типа Sd-орбитали расщепляются сильнее, чем 4 -орбитали; естественно, что расщепление и тех и других орбиталей больше, чем расщепление Sd-орбиталей ( см. стр. [39]
 |
Виды гибридизации и соответствующие им структуры комплексов. [40] |
Эта теория рассматривает воздействие лигандов на d - орбитали иона-комплексообразовате-ля. Форма и пространственное расположение d - орбиталей представлены ранее на рис. 1.7. В свободном атоме или ионе энергии всех d - электронов-принадлежащих к одной и той же электронной оболочке, одинаковы - эти электроны занимают один энергетический уровень. Лиганды, присоединяемые к положительному иону-комплексообразователю, могут быть или отрицательными ионами, или полярными молекулами, которые обращены к комплексообразователю своим отрицательным концом. Между электронными облаками d - электронов и отрицательными лиганцами действуют силы отталкивания, приводящие к увеличению энергии d - электро-нов. Энергия электронов на d - орбиталях, расположенных близко к лигандам, возрастает больше, а на rf - орбиталях, удаленных от лигандов, меньше; в результате под действием лигандов происходит расщепление энергетических уровней d - орбиталей. [41]
Эта теория рассматривает воздействие лигандов на с. В свободном атоме или ионе энергии всех d - электронов, принадлежащих к одной и той же электронной оболочке, одинаковы - эти электроны занимают один энергетический уровень. Лиганды, присоединенные к положительному иону, являются или отрицательными ионами, или полярными молекулами, повернутыми к комплексообразователю своим отрицательным концом. Между электронными облаками ( / - электронов и отрицательными лигандами действуют силы отталкивания, приводящие к увеличению энергии rf - электронов. Однако воздействие лигандов на различные о. Энергия электронов на rf - орбиталях, расположенных близко к лигандам, возрастает больше, а на d - орбиталях, удаленных от лигандов, меньше - под действием лигандов происходит расщепление энергетических уровней d - орбиталей. [42]
 |
Виды гибридизации и соответствующие им структуры комплексов. [43] |
Эта теория рассматривает воздействие лигандов на d - орбнтали иона-комплексообразовате-ля. Форма и пространственное расположение d - орбиталей представлены ранее на рис. 1.7. В свободном атоме или ионе энергии всех d - электронов, принадлежащих к одной и той же электронной оболочке, одинаковы - эти электроны занимают один энергетический уровень. Лиганды, присоединяемые к положительному иону-комплексообразователю, могут быть или отрицательными ионами, или полярными молекулами, которые обращены к комплексообразователю своим отрицательным концом. Между электронными облаками d - электронов и отрицательными лиганцами действуют силы отталкивания, приводящие к увеличению энергий d - электро-нов. Однако воздействие лигандов на различные rf - орбитали неодинаково. Энергия электронов на d - орбиталях, расположенных близко к лигандам, возрастает больше, а на с / - орбиталях, удаленных от лигандов, меньше; в результате под действием лигандов происходит расщепление энергетических уровней d - орбиталей. [44]
Страницы: 1 2 3