Реакционная диффузия
Cтраница 3
В зависимости от природы образующихся в диффузионном слое фаз различают атомную и реакционную диффузию. Атомная диффузия - это диффузия элементов в твердом растворе или химическом соединении переменного состава, изменяющая только их концентрацию. [31]
Таким образом, из результатов работы [174] следует, что в механизме реакционной диффузии при воздействии паров серы на медь при высоких температурах главную роль играет диффузия меди на наружную поверхность окалины, где главным образом и происходит наращивание окалины. Диффузия серы в обратном направлении играет в общем процессе второстепенную, хотя и заметную роль. Слой CuaS наращивается как со стороны металла, так и на границе с наружным слоем. [32]
Точка пересечения функций Фг TIL Ф2 на рис. 1 соответствует истинному значению коэффициента реакционной диффузии - Оист. [33]
Распространяя эти представления на реакционную диффузию, автор приходит к выводу, что величина Е при реакционной диффузии также определяется стабильностью соответствующих электронных конфигураций взаимодействующих атомов; в то же время скорость диффузии преимущественно определяется активностью электронного обмена между атомами и его направлениями. [34]
Сплошные карбидные структуры возникают в результате непосредственного химического взаимодействия металла с углеродом разлагающейся при трении смазки путем реакционной диффузии. Для образования карбидов совершенно не обязательно нагревание поверхностных слоев до температур, превышающих точку фазового перехода ( в аустенит), как и охлаждение с большой скоростью. В связи с этим появления карбидных слоев при трении можно ожидать при умеренных температурах и на любых карбидообразу-ющих металлах и их сплавах, в том числе таких, которые в твердом состоянии углерод не растворяют. [35]
Таким образом, наблюдения автора согласуются с положениями Д. А. Прокошкина и А. А. Попова о последовательности возникновения и росте фаз при реакционной диффузии. [36]
Распространяя эти представления на процессы реакционной диффузии, сопровождающейся образованием химических соединений, можно полагать, что энергии активации реакционной диффузии определяются также стабильностью соответствующих электронных конфигураций атомов партнеров в процессе диффузии, концентрацией коллективизированных электронов и способностью атомов приобретать стабильные конфигурации в результате диффузии. В то же время скорость диффузии преимущественно определяется активностью электронного обмена между атомами партнеров и его направлением. [37]
При изучении [19] зоны взаимодействия между никелем и SiC в зависимости от концентрации легирующих добавок было выявлено интенсивное развитие процесса реакционной диффузии. [38]
С изложенной точки зрения можно интерпретировать и процессы, совершающиеся при образовании покрытий из тугоплавких соединений, что связано с реакционной диффузией. Чем стабильнее электронная конфигурация последнего, тем, очевидно, выше должна быть энергия активации реакционной диффузии. В результате получения переходным металлом электронов металлоида статистический вес й5 - состояний атома металла в соединении становится выше, чем в собственном металле. Этот контраст является движущей силой диффузии, которая соответственно приобретает передаточный характер - происходит переход атома неметалла из образовавшегося соединения в более глубоко лежащий слой атомов переходного металла вновь с образованием соединения. Этот переход является следствием перехода остова атома металла из собственно металла в слой образовавшегося химического соединения с увеличением числа й-электронов остова металлического атома, входящего в это соединение. Электронная конфигурация этого последнего атома становится более стабильной. В случае карбидизации титана углерод передает часть электронов атому титана, у которого в связи с этим конфигурация становится более стабильной, и стремится достроиться до еще большего статистического веса й5 - состояний за счет атомов титана, находящихся в металле, перемещающихся вследствие этого в слон карбида, освобождая места для атомов углерода. В случае борирования титана вследствие меньшей стабильности конфигураций бора ( по сравнению с углеродом) последний передает большое число электронов атому титана, поэтому требуется меньшее число атомов титана из металла для достижения некоторого статистического веса 5-состояний атомами титана в бориде. [39]
Для системы РЬ2МоО5 / МоО3 установлен различный характер воздействия давления кислорода в газовой фазе на ПРД ( s) и на реакционную диффузию в месте контакта реагентов ( С), что указывает на различия в механизме реакционной диффузиии по поверхности и в месте контакта. [40]
Легирование материалов алюминиевой заготовки кремнием, марганцем и другими элементами, а стали - ванадием, титаном, кремнием и никелем повышает энергию активации реакционной диффузии. Их влияние связано с затруднением образования зародышей в промежуточной фазе. Противоположное влияние оказывают углерод и марганец в стали. Повышенное содержание в определенных пределах в стали свободного кислорода и азота ведет к росту температуры начала образования интерметаллидов. Возникновение интерметаллидного слоя для каждой температуры начинается после некоторого критического времени, т.е. имеет место латентный период TO, по прошествии которого интенсивно образуются ин-терметаллиды. [41]
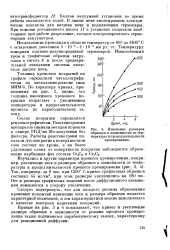 |
Изменение размеров образцов в зависимости от температуры и продолжительности хромирования. [42] |
Кривые на рис. 3 и 4 показывают, что привес и увеличение размера образцов в зависимости от режима процесса хромирования также подчиняется параболическому закону, характерному для реакционной диффузии. [43]
Особенно большое значение процессы гетеродиффузии имеют для формирования сварных соединений разнородных сталей и разнородных металлов, так как обычные закономерности диффузионного процесса осложняются специфическими условиями диффузии - реакционной диффузией и диффузией, вызванной влиянием состава на изменение термодинамической активности растворенного и диффундирующего вещества. [44]
Подобный суммарный процесс, в котором, наряду с перемещением частиц внутри однородных областей под влиянием градиента химического потенциала, имеет место взаимодействие их, сопровождающееся переходом одних фаз в другие, называют реакционной диффузией. [45]
Страницы: 1 2 3 4