Pt-электрод
Cтраница 2
Если титруют обратимую на Pt-электроде пару ( например, J2 - 2J -) реагентом, представляющим собой необратимую окислительно-восстановительную систему ( например, тиосульфат - тетратионат, 820 - S4O -), то ток проходит лишь до наступления конечной точки титрования, а в конечной точке и после нее ток равен или близок к нулю. [16]
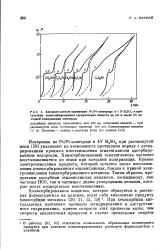 |
Анодные кривые заряжения Pt / Pt-электрода в 1 N Н ЗО в присутствии хемосорбированных органических веществ до ( а и после ( б катодной поляризации электрода. [17] |
Измерения на Pt / Pt-электроде в iN H2S04 при разомкнутой цепи [59] указывают на возможность протекания наряду с дегидрированием процесса восстановления этиленгликоля адсорбированным водородом. Хемосорбированный этиленгликоль частично восстанавливается до этана при катодной поляризации. Кривая электроокисления продукта, который остается после восстановления хемосорбированного этиленгликоля, близка к кривой электроокисления хемосорбированного метанола. Таким образом, продуктами адсорбции этиленгликоля являются, по-видимому, как частицы НСО, так и частицы с двумя углеродными атомами, которые могут подвергаться восстановлению. [18]
Объясняется это [226, 227] заполнением поверхности Pt-электрода адсорбированными свободными лигандами, которые блокируют часть поверхности электрода. [19]
ТЭ индицируют амперометрически с применением Pt-электродов при разности потенциалов 150 мв. [20]
 |
Кривые смещения потенциала Pt / Pt-электрода после. [21] |
Кривые смещения потенциала Pt / Pt-электрода после введения НСООН аналогичны соответствующим кривым для метанола. Однако в растворах НСООН накапливается примерно в два раза больше адсорбированного продукта при ф2 - - 500 мв ( fe 0 90), чем в растворах СН3ОН, и, в отличие от последних, заметные количества адсорбированного продукта ( k - 0 45) обнаруживаются в случае ср 60 мв. [22]
С в аппарате Гитторфа с Pt-электродами до тех пор, пока через него не прошло 0 0100 фарадея электричества. [23]
Кинетика адсорбции органических веществ на Pt-электродах различной дисперсности удовлетворительно описывается соотношениями, отвечающими адсорбции на равномерно-неоднородной поверхности. [25]
Для снятия кривой заряжения Pt / Pt-электрода используется ячейка, изображенная на рис. 3.23. Приготовление платинированного платинового электрода описано в § 1.1. Раствор 0 5 М H2SO4 готовят из дважды перегнанной под вакуумом серной кислоты и бидистилля-та. При снятии кривых заряжения необходимо соблюдать такую последовательность операций. [26]
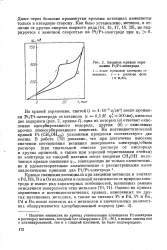 |
Анодные кривые заряжения Pt / Pt-электрода. [27] |
Наличие минимума на кривых установления потенциала Pt-электрода в растворах метанола, который был обнаружен в [78-80], в наших опытах как с платинированной, так и с гладкой платиной, не было подтверждено. [28]
Ионы цинка ( II) на Pt-электроде в кислой среде неэлектроактивны, между тем как ионы гексацианоферрата ( III) восстанавливаются под действием катодного тока до ионов гексацианоферрата ( II), которые химически взаимодействуют с ионами цинка ( II) с образованием малорастворимого осадка. [29]
Вещество, хемосорбирующееся на Pt / Pt-электроде в растворах формальдегида, ведет себя подобно хемосорбированному метанолу. [30]
Страницы: 1 2 3 4 5
