Pt-электрод
Cтраница 4
Особого внимания заслуживает тот факт, что при контакте Pt / Pt-электрода с растворами пропанола ( опыт 3 в табл. 1) в газовой фазе появляется бутан, который следует рассматривать как продукт частичной рекомбинации радикалов С2Н5, первоначально образующихся при разрыве Q - С2 - связи. [46]
Титрование Gr ( VI) выполняют по току окисления Н202 с Pt-электродом при потенциале 1 0 в ( отн. [47]
Представляло интерес исследовать поведение сернокислого гидро-ксиламина ( ГА) на Pt / Pt-электроде, для которого наиболее характерны процессы адсорбции и хемосорбции изученных выше веществ. Интересно, что гидроксиламин ведет себя подобно нитрометану и метилгидро-ксиламину. [48]
Метод основан на регистрации и усилении окислительно-восстановительного потенциала пары NOg I NOg на инертном Pt-электроде. Потенциал стабильно измеряется в интервале содержания нитрита от 0 7 - 0 28 г / л при сочленении со стандартным каломельным электродом сравнения. При показании ниже 250 мв открывается магнитный клапан и в ванну подается раствор нитрита определенной концентрации, пока сигнал не достигнет прежнего значения. [49]
Из этих данных следует, что изотоп кислорода О18, введенный в поверхностные окислы Pt-электрода, образующихся при потенциале. Обмен кислорода окислов с электролитом может привести только к уменьшению наблюдаемого эффекта. Полученные данные позволяют сделать заключение об участии высших поверхностных кислородных соединений платины в реакции электрохимического выделения кислорода. [50]
При очень высоких концентрациях хлоридов бромид-ионы целесообразно определять методом ПТ раствором гипохлорита натрия по Pt-электроду. Промежуточный интервал не пригоден для анализа, так как эквивалент брома имеет переменное значение. [51]
На рис. IV.4 приведены катодные хронопотенциограммы, снятые при различных плотностях поляризующего тока на Pt-электроде. Линейная зависимость между Е и lg [ ( tj / - f Y / t1 ] с наклоном 62 мВ, положение которой не изменяется при изменении плотности включаемого тока, свидетельствует о практически обратимом протекании электродной реакции (IV.93) в указанных условиях. Катодные и анодные хронопотенциограммы, полученные с растворами, содержавшими комплексы 1гС1Г и 1гС1 § -, также подчиняются уравнению обратимой хронопотенцио-метрической волны. [53]
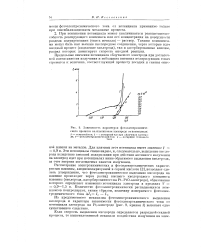 |
Зависимость параметров фотоэлектрохимического процесса на платиновом электроде от потенциала. [54] |
Из предложенного механизма фотоэлектрохимичсского выделения кислорода и характера зависимости фотоэлектрохимического тока от потенциала электрода на Pt-электроде ( рис. 9, кривая 3) вытекает одно существенное следствие. [55]
Исследуемый газ и раствор 0 02 N KJ ( электролит) подают в стеклянную трубку с индикаторными Pt-электродами. Генерируемый на электродах иод вступает в реакцию с компонентами газа, а его избыток определяется с помощью индикаторных электродов. [56]
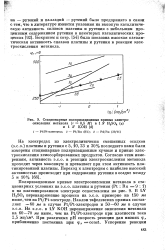 |
Стационарные поляризационные кривые алектро. [57] |
В iN H2S04 перенапряжение процесса на э.с.о. примерно на 150 мв ниже, чем на Pt / Pt-электроде. [58]
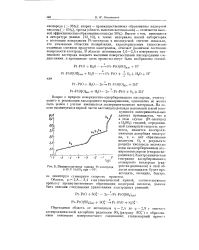 |
Поляризационная кривая Pt-электрода в 10 N H2S04 при - 70. [59] |
Вместе с тем, имеющиеся в литературе данные [12, 13], а также материалы нашей лаборатории о состоянии поверхности Pt-электрода в исследуемой системе показали, что указанным областям поляризации, характеризуемым существенно отличным составом продуктов электролиза, отвечает различное состояние поверхности электрода. [60]
Страницы: 1 2 3 4 5
