Окисляющее действие - азотная кислота
Cтраница 1
Окисляющее действие азотной кислоты обусловливается восстановлением иона азота. Степень восстановления зависит от концентрации азотной кислоты и природы окисляемого вещества. Обычным продуктом восстановления азотной кислоты является окись азота NO, но часто образуются и другие продукты, как двуокись азота, закись азота, элементарный азот и даже аммиак. [1]
Окисляющее действие азотной кислоты сказывается и на неметаллах. [2]
Для усиления окисляющего действия азотной кислоты к ее водному раствору прибавляют HCI. Смесь из трех частей НС1 и одной части HNO3 царская водка - при нагревании выделяет хлор и нитрозил-хлорид NOC1 ( HNO3 3HC1 - 2Н2О С12 NOC1), под действием которых растворяются даже платина и золото. [3]
Сульфогруппы стабилизуют молекулу и предохраняют от окисляющего действия азотной кислоты, а поскольку реакция сульфирования обратима, то сульфогруппы легко замещаются затем нитрогруппами. [4]
Серная кислота значительно ускоряет реакцию этернфикацни и уменьшает окисляющее действие азотной кислоты. [5]
Вместе с тем повышается устойчивость бензольного ядра к окисляющему действию азотной кислоты, так как ациламиногруппа менее сильно активирует ядро, чем свободная аминогруппа. [6]
Преимущество серной кислоты в том, что она понижает окисляющее действие азотной кислоты. Высокая температура кипения серной кислоты позволяет в случае необходимости проводить нитрование при высокой температуре. Немаловажное преимущество нитрующей смеси перед азотной кислотой состоит в том, что она может храниться в железной аппаратуре, так как не вызывает коррозии железной и чугунной аппаратуры, что очень важно в заводской практике. [7]
Нитрование аминов проводят в особых условиях, так как аминогруппа очень чувствительна к окисляющему действию азотной кислоты. Поэтому нитрование аминосоединений ведут при очень низких температурах. В большинстве случаев аминогруппу защищают от окисления, заменяя в ней атом водорода на остаток органической кислоты. Эта реакция называется ацилированием. Полученный в результате ацилирования амина продукт не окисляется азотной кислотой и не теряет способности к нитрованию. [8]
Из всех указанных реакций в первую очередь должно быть проведено нитрование для того, чтобы не потребовалась защита функциональных групп пиридоксина от окисляющего действия азотной кислоты. [9]
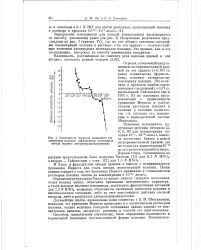 |
Зависимость скорости выделения ( растворения полония от величины потенциала катода ( кривая диспропорционирования. [10] |
Отклонение результатов Хилла от наших данных ( порядка нескольких сотых вольта) можно объяснить причинами методического характера, а столь высокое значение потенциала, полученное французскими авторами для 1 57VHN03, возможно, объясняется частичным переходом полония в шестивалентное состояние, либо за счет окисляющего действия азотной кислоты, либо в результате диспропорционирования. [11]
Параллельно с этерификацией гидроксильных групп целлюлозы могут развиваться также: а) гидролиз макромолекулы целлюлозы под влиянием кислот и воды, что приводит к уменьшению молекулярной массы и, следовательно, вязкости растворов целевого продукта; б) образование сульфоэфиров целлюлозы, так как в нитрующей смеси присутствует серная кислота; в) образование окси-целлюлозы за счет окисляющего действия азотной кислоты. Процесс нитрования целлюлозы проводят таким образом, чтобы все побочные и нежелательные реакции свести к минимуму. [12]
Действительно, в продуктах нитрования можно обнаружить спирты, обычно в количествах значительно меньших, чем можно было ожидать теоретически. Это и неудивительно, учитывая сильно окисляющее действие азотной кислоты. [13]
Наряду с каталитическим действием на гидролиз образующаяся азотная кислота оказывает и окисляющее действие. Однако при тех концентрациях, которые уже сильно влияют на гидролиз, окисляющее действие азотной кислоты особенно в отсутствии окислов азота еще относительно слабо. По-видимому, когда гидролиз закончился, концентрация азотной кислоты оказывается уже достаточной для значительного убыстрения окисления тем более, что одновременно возросла и концентрация динитрогли-церина, окисляющегося легче, чем нитроглицерин. [14]
Заместители в ароматическом или гетероциклическом ядре, с одной стороны, облегчают, а с другой - затрудняют прямое нитрование. Влияние метальных групп сравнительно мало заметно; сильнее влияние более длинных цепей, причем в этом случае особенно сильно проявляется окисляющее действие азотной кислоты. Наибольшей реакционной способностью обладают фенолы и амины, а также галогензамещенные соединения. Напротив, трудно нитруются карбоновые кислоты, сульфэкислотыисами нитросоеди-нения. В отношении образования изомеров найдены не наблюдаемые в других случаях отклонения и закономерности. [15]
Страницы: 1 2 3