Алкоголиз
Cтраница 2
Алкоголиз целлюлозой эфиров сильных карбоновых кислот протекает с разрывом только алкил-кислородной связи и образованием простого эфира целлюлозы. Так, алкоголиз целлюлозой метилового эфира перфтормасляной кислоты ( Й25 6 8 - 10 -) приводит к образованию метилового эфира целлюлозы, содержащего лишь очень незначительное количество перфторбутирильных групп. [16]
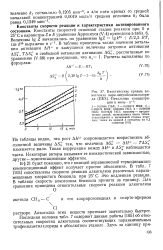 |
Кинетические кривые ал-коголиза / шра-нитробензоилхлори-да ( ПБХ. Начальные концентрации в моль - л 1. [17] |
Алкоголиз этих веществ протекает значительно быстрее. Последняя колонка табл. 7 содержит данные работы [105] об относительных скоростях алкоголиза соответствующих паразамещенных трифенилметилхлорида в абсолютном этаноле. [18]
Алкоголиз целлюлозой эфиров сильных карбоновых кислот протекает с разрывом только алкил-кислородной связи и образованием простого эфира целлюлозы. Так, алкоголиз целлюлозой метилового эфира перфтормасляной кислоты ( kK 6 8 - 10 -) приводит к образованию метилового эфира целлюлозы, содержащего лишь очень незначительное количество перфторбутирильных групп. [19]
Алкоголиз целлюлозой фенил -, р-хлорэтил - или р-фторэтилфос фита протекает при температуре 100 - 130 С; при этом образуются кислые эфиры целлюлозы и соответствующих алкилфосфористых кислот с у 60 - 80 из. [20]
Алкоголиз ( схема 87) широко применяется для превращения жирных кислот, входящих в состав липидов, в метиловые эфиры, минуя стадию образования свободных кислот, и для получения частично этерифицированных глицеридов реакцией триглицерида с глицерином. [21]
Алкоголиз может быть осуществлен путем обработки полиэфира этиленгликолем. Этим методом в качестве продукта реакции получается непосредственно диэтиленгликольтерефталат, который после очистки можно использовать для получения полиэтилентерефталата. [22]
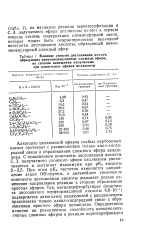 |
Влияние степени диссоциации кислот. [23] |
Алкоголиз целлюлозой эфиров слабых карбоновых кислот протекает с расщеплением только ацил-кисло-родной связи и образованием сложного эфира целлюлозы. [24]
Алкоголиз и аминолиз хлорангидридов сульфокислот, протекающий с образованием сложных эфиров и соответственно амидов сульфокислот, может быть сопоставлен с соответствующими реакциями галогенангидри-дов карбоновых кислот. Сульфохлориды, однако, как правило, менее реак-ционноспособны ( почему. Так, в холодной воде сульфохло-риды разлагаются лишь медленно, а некоторые из них можно даже перекристалл изовывать из воды. [25]
Алкоголиз и переэтерификация могут происходить также под влиянием свободных гидроксильных и карбоксильных групп, имеющихся в продуктах конденсации многоосновных кислот и многоатомных спиртов. [26]
Алкоголиз, гидролиз и другие реакции хлоркремнийгидридов [38, 45, 157, 162, 163, 193, 511, 532, 563, 565, 580, 589, 598-626], приводящие к образованию алкокси -, арокси -, ацилокси - и алкилмеркаптокремний-гидридов и силанолов, изучены подробнее реакций аммонолиза. [27]
Алкоголиз галогенидов, сульфатов и сульфонатов для получения простых эфиров имеет почти столь же общее значение, что и реакция гидролиза. Эта реакция сопровождается теми же побочными реакциями и теми же изменениями в реакционной способности в зависимости от структуры субстрата реакции. В качестве нуклеофилов часто используют алко-голяты, причем родоначальный спирт обычно служит растворителем. [28]
Алкоголиз диалкилбериллиев также протекает весьма бурно. Метиловый и изопропиловый спирты реагируют с диэтилбериллием при - 80 С весьма энергично; реакция с этиловым спиртом протекает более спокойно. [29]
Алкоголиз ангидридов и хлорангидридов кислот благодаря их сильно повышенной карбонильной активности проходит гораздо легче, чем алкоголиз карбоновых кислот или сложных эфиров. Тем не менее и в этом случае кислоты и основания оказывают ускоряющее действие. Это каталитическое влияние особенно заметно у несколько менее реакционноспособных ангидридов. [30]
Страницы: 1 2 3 4