Алкоголят - металл
Cтраница 3
Спирты и карбоновые кислоты, в которых водород является активным, вступают во взаимодействие с металлом, образуя алкоголяты металлов или соли. Эта реакция характерна, в основном, для металлов щелочной труппы ( Na, К), а также для алюминия. [31]
Интенсивное дегидрохлорирование ПВХ могут катализировать некоторые группы соединений металлов, в частности щелочи, а также амиды или алкоголяты металлов. Если ПВХ, растворенный в тетрагидрофуране, обрабатывать при комнатной температуре амидом натрия в жидком аммиаке или суспензию ПВХ в жидком аммиаке - амидом калия или натрия при 20 С под некоторым давлением, то образуется полностью дегидрохлорированный ( С: Н 1) не растворимый в бензоле полимер черного цвета с температурой плавления 400 - 410 С, который дает четкий сигнал ЭПР: синглет с A msl 7 - 12 гс. [32]
В трех патентах, выданных Борроусу и Стюарту [69-71], описана полимеризация и сополимеризация окисей олефинов в присутствии алкоголятов металлов, принадлежащих ко 2 - й и 3 - й группам периодической таблицы элементов. Алкоголяты этих металлов сами по себе не являются высокоактивными катализаторами полимеризации окисей, однако они входят в качестве активных компонентов в различные каталитические системы, обладающие высокой активностью. Даже при более высоких температурах и относительно большой продолжительности полимеризации степень конверсии, как правило, невысока. [33]
Амиды Y -, 6 - и е-галогенокислот циклизуются под действием таких оснований, как аммиак, водная щелочь или алкоголяты металлов, напр. [34]
Амиды у -, о - и е-галогенокислот циклизуются под действием таких оснований, как аммиак, водная щелочь или алкоголяты металлов, напр. [35]
Алкилнрованне таких соединений, как р-дикетоны, р-кетоэфиры и эфиры малоновой кислоты, можно проводить в спиртовых средах в присутствии алкоголятов металлов в качестве оснований - При наличии двух электроноакиепторнмх заместителей отрыв протона от углеродного атома, находящегося между ними. [36]
Как - дикетонь - кетоэфкры: и-эфиры: малонрвой кислота, можно проводить в спиртовйх средах - в присутствий; алкоголятов металлов & качестве основ з кий. При - на линиггдвух электреноаКцепторнйх заместителей / отрыв протона - от / углеродного атома, находящегося между ними, благоприятствует: образованию единственного еяоля га, алкилирование которого затем проходит по 5 2-ме-ханизму. [37]
Последовательное отщепление нескольких молекул олефи-на имеет место в катионах полиалкилсодержаших соединений элементов III, IV ( табл. 18), V групп и алкоголятов металлов. Отметим, что в масс-спектрах SiEt4 и GeEt4 на долю ионов, образующихся по типу Л, приходится больше половины ионного тока. [38]
Среди многочисленных классов соединений, которые могут быть получены из неорганических веществ, в газовой хроматографии можно использовать лишь некоторые, например карбонилы металлов, алкоголяты металлов, ме-таллалкилы и несколько типов хелатов металлов. Среди этих классов соединений особый интерес представляют хелаты, поскольку можно получить хелаты практически любого металла. Более того, получить хелаты с количественным выходом значительно легче, чем другие соединения, и они меньше подвержены гидролизу. Хелатообра-зующие лиганды содержат донорные атомы таких элементов, как кислород, сера, селен, фосфор и азот. Содержащие в качестве доиорных атомов кислород ( З - дикетоны образуют хелатные соединения металлов, летучесть, растворимость и термическая стойкость которых удовлетворяют требованиям газовой хроматографии. [39]
Направление научных исследований: выращивание кристаллов в растворах; гравиметрический анализ; полярография неводных растворителей; полярография комплексов благородных металлов с органическими лигандами; газовая хроматография; очистка неорганических солей, контролируемая радиоактивными индикаторами; спектроскопия неорганических комплексов; химия алкоголятов металлов; методы и механизм восстановления органических соединений гидридами металлов; металлорганиче-ские соединения; замещенные фенолы; бензальдегид; синтез меченой индолилуксусной кислоты и применение ее в изучении физиологии растений. [40]
Алкоголяты металлов обычно представляют собой основания, достаточно сильные для того, чтобы их можно было применять при алкилировании малоновых и циапуксуспых эфирпв, нитрилов малоновой кислоты и некоторых мононитрилов. Применяемые обычно алкоголяты металлов можно расположить по возрастающей основности в следующий ряд [34-37]: CH3ONa CHaCHi0Na ( CH. [41]
Подробно влияние различных катализаторов на свойства полиметилфенилсилоксанов и протекающие в их присутствии процессы отверждения рассмотрены М. Б. Фромбергом [ 11, с. В качестве катализаторов применялись алкоголяты металлов, амины, металлсодержащие сиккативы. [42]
Можно применять органические основания, например пиридин, пиперидин, морфолим, этанолампп и др.; неорганические основания, например едкий натр, едкое кали, гидроокись бария и др.; кроме того, могут применяться вещества, реагирующие как щелочи вследствие1 гидролиза, такие, как карбонат натрия, карбонат калия, бикарбонат натрия, ацетат натрия. Очень эффективными реагентами являются алкоголяты металлов, особенно метилат и этилат натрия, получающиеся растворением металличесюго натрия в соответствующем спирте; их вводят в реакцию с омыляемыми соединениями в отсутствие влаги. [43]
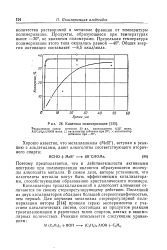 |
Кинетика полимеризации. [44] |
Поэтому предполагается, что в действительности активными центрами при полимеризации являются образующиеся молекулы алкоголята металла. В самом деле, авторы установили, что алкоголяты металла могут быть эффективными катализаторами, способствующими образованию кристаллического полимера. Катализаторы триалкилалюминий и алкоголят алюминия отличаются по своему стереорегулирующему действию. Последний из двух катализаторов обладает большей стереоспецифичностью, чем первый. [45]
Страницы: 1 2 3 4