Алкоксирадикал
Cтраница 2
Сделано предположение, что при рекомбинации пероксиради-калов образуются алкоксирадикалы. [16]
Сделано предположение, что при рекомбинации пероксиради-калов образуются алкоксирадикалы, которые ведут далее цепь окисления, передавая ее при взаимодействии с гидроперекисью, что ускоряет распад последней по сравнению с разложением в инертной атмосфере. [17]
Таким образом, внесение ароматического радикала или удлинение алкоксирадикала до бутила в положении 5 у фу-ран-2 - карбоновой кислоты ведет к повышению никотииолити-ческой активности. [18]
Это можно объяснить тем, что отрыв водорода алкоксирадикалом и образование углеводородных радикалов в таких случаях сопровождается аллилыюй перегруппировкой ( см. также стр. [19]
Эфиры ч, р-ненасыщенных кислот с функциональным группами в алкоксирадикале / / Журн. [20]
В условиях малых скоростей скольжения длина алкильных групп в алкоксирадикалах всех синтезированных эфиров не оказывает существенного влияния на их активность. [21]
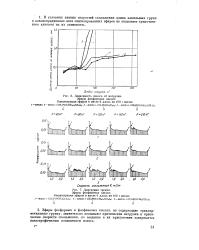 |
Зависимость износа от нагрузки.| Диаграмма трения. Эфиры фосфиновых кислот. [22] |
В условиях низких скоростей скольжения длина алкильных групп в алкоксирадикалах всех синтезированных эфиров не оказывает существенного влияния на их активность. [23]
Поляризация в продуктах реакции, влияние вязкости среды, р-распад алкоксирадикалов, перехват радикалов в растворе стиролом - все указывает на радикальный механизм реакции. Кинетические измерения показывают, что стадия переноса электрона с реактива Гриньяра на перекись определяет кинетику всей реакции. Линейность следует рассматривать как доказательство стадии переноса электрона в этой реакции. [24]
Второе направление реакции продолжения цепи - распад втор-бутилпероксида с образованием алкоксирадикалов и продуктов с меньшим числом углеродных атомов - ацетальдегида, ацетона, этанола, метанола. [25]
Данные по изучению холинолитического действия амино-эфиров в связи со строением алкоксирадикала дают следующую картину действия. В случае увеличения или укорочения алкоксирадикала на один углерод наблюдается падение активности у препаратов с нормально амиловым и пропило-вым радикалами соответственно. [26]
Следующей стадией является гемолитический распад гидроперекиси с образованием двух радикалов - алкоксирадикала, соответствующего гидроперекиси, и а-оксиалкоксирадикала, производного от оле-фина. Их взаимодействие, проходящее с отрывом протона, приводит к а-оксикетону. [27]
Можно было бы ожидать, что получение эфиров возможно путем присоединения свободных алкоксирадикалов к олефинам ( или кар -, бониевым ионам) или путем замещения в алканах. По-видимому, радикалы инициируют полимеризацию олефинов или разлагаются сами. [28]
Возникающее распределение электронов означает, что п л - возбужденные состояния напоминают алкоксирадикалы, поскольку имеют достаточно электрофильный кислород и нуклео-фильные карбонильные атомы углерода. [29]
Возникающее распределение электронов означает, что п л - возбужденные состояния напоминают алкоксирадикалы, поскольку имеют достаточно электрофильный кислород и нуклео-фильные карбонильные атомы углерода. В ароматических и а р-непредельных альдегидах значительно сильнее выражен я - - я - переход, обладающий сходной энергией, так что эти соединения могут вступать в реакции как в п п -, так и в п л - состоя-нии; последнее характеризуется меньшей электрофильностыо атомов кислорода, что понижает его способность отщеплять атом водорода от субстрата. [30]
Страницы: 1 2 3 4