Алкоксисилан
Cтраница 1
Пиролиз алкоксисиланов производят при температуре 700 - 750 С в кварцевых реакторах горизонтального прямоточного типа. Во входную магистраль установки включают барботер с алкоксисиланом, пары которого увлекаются в зону реакции потоком аргона или азота. [1]
Реакция алкоксисиланов с органодигидроксисиланами ( реакция ( 16)) протекает в присутствии щелочных или кислых катализаторов, например силанолятов натрия, и может служить для синтеза циклов. [2]
Расщепление алкоксисиланов проходит главным образом по связи кремний - кислород, а не углерод - кислород. [3]
Из алкоксисиланов, способных к полимеризации по схеме ( 2) ( стр. При добавке 0 5 % перекиси бензоила время полимеризации сокращается до 25 час. [4]
Взаимодействие алкоксисиланов с кислотами бора часто протекает неоднозначно, а направление реакций сильно зависит от строения алкоксисилана. Сведения о реакциях этого типа иногда противоречивы. [5]
Взаимодействие алкоксисиланов с борным ангидридом приводит к образованию триалкилборатов и боросилоксанов. [6]
Взаимодействие алкоксисиланов со сложными эфирами протекает по схеме трансэтерификации с образованием новых алкоксисиланов и сложных эфиров. [7]
Смеси алкоксисиланов с гидросиланами либо индивидуальные алкоксигидросиланы склонны к каталитической равновесной перегруппировке с преимущественным образованием соединений с одинаковыми функциями. [8]
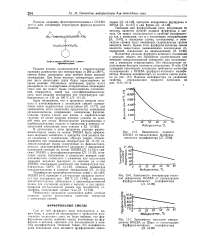 |
Зависимость температуры тепловой деформации DGEBA от концентрации фурфурол-кетонного модификатора [ Л. 13 - 90 ]. [9] |
Реакция низших алкоксисиланов с гидроксильными группами развивается при температурах от 200 до280 С, причем более громоздкая цепь требует более высокой температуры. При более высоких температурах некоторая часть эпоксидных групп будет израсходована во время реакции. [10]
При использовании алкоксисиланов повышение температуры до оптимальной в большинстве случаев приводит к повышению прозрачности пленок окислов элементов IV группы. При получении пленок из растворов нитратов, например Тп ( МОзЬ, с повышением температуры до 500 - 600 С также наблюдается улучшение прозрачности пленок. При 500 - 600 С завершается полное разложение нитратов и пленки приобретают постоянный состав, отвечающий чистой ThOz - Химическим анализом доказано, что после прокаливания Th ( OH) 4, полученной гидролизом спиртового раствора Th ( NO3) 4 при 600 С, ионы МОз отсутствуют. Для иона КОз известны собственные полосы поглощения в области Я 302 и 194 нм [275], поэтому до тех пор, пока в составе пленки присутствуют еще остатки неразложившихся нитратов, пропускание ее занижено. Термическая зависимость спектрального пропускания пленок, образованных хлоридами, обратная. [11]
Из числа алкоксисиланов особенно опасными являются мет-оксипроизводные органосиланов. Так, тетраметоксисилан вызывает некроз клеток роговицы глаза, что может привести к слепоте. По-видимому, в этих случаях вредное действие на организм человека оказывает метиловый спирт, получающийся при гидролизе. Метоксипроизводные, однако, более токсичны, чем метиловый спирт. Тетраэтоксисилан заметно менее токсичен; при его вдыхании проявляется только гемолитическое действие. Он вызывает также раздражение слизистых оболочек носа, глаз, может действовать как наркотик. [12]
Химические свойства алкоксисиланов определяются наличием в них реакционноспособных связей Si - Н и Si-OR. Эта реакция катализируется металлическим натрием или его этилатом и используется для получения силана. [13]
Реакция гидролиза алкоксисиланов подвержена кислотному и основному катализу, причем гидролиз некоторых алкоксисиланов с разветвленными алкоксидными заместителями идет только в присутствии катализаторов. [14]
Для фторирования алкоксисиланов обычно используют 48 % - ную плавиковую кислоту. [15]
Страницы: 1 2 3 4