Аллилбензол
Cтраница 3
Рамар-Люка и Амага [34], изомеризуя аллилбензол в пропенилбензол над инфузорной землей при 500, доказали возможность миграции двойной, связи и превращения аллильных производных в пропенильные путем нагревания. Смакула [36] обнаружил изомеризацию транс-стильбена ( С6Н5 СН: СН С8Н8) в цис-стильбен под действием света в растворе гексана. Он предполагал, что первичный процесс заключается в ослаблении этиленовой. [31]
О полимеризации виншщиклогексана, аллилциклогексана, аллилбензола, 4-фенилбутена - 1.5 - фенилпентена-1 см. также СШ ] С. [32]
Следует отметить, что выход с аллилбензолом очень мал. В случае двух алкильных групп в катионе ( соединение 3) нитрилиевый катион оказывается более стабильным. [33]
Леви и Коп [21] алкилировали натриевую соль аллилбензола бромистым аллилом, хлористый. [34]
Менее плоско расположены, вероятно, молекулы аллилбензола. Падение величины т для н-продилбен-зола связано, пр-видимому, с меньшей плотностью его монослоя по сравнению с другими исследованными углеводородами. Расположение молекул исследованных углеводородов яа окиси алюминия параллельно поверхности сохраняется также с ростом температуры. [35]
Это действительно например для пропенил - и аллилбензолов и продуктов их замещения; пропе-ниловые соединения обладают наибольшей скоростью реакции. [36]
Этот вид изомеризации, типичный для производных аллилбензола, представляет собой 1 3-перемещение аллильной системы. В данном примере двойная связь мигрирует в положение, где она становится сопряженной с циклом. [37]
Наибольшей интенсивностью пика ионов с массой 91 отличается аллилбензол, где этому процессу способствует ослабление р-связи относительно ароматического ядра. [38]
Рассчитаны значения энергии активации реакций гидрирования стирола, аллилбензола и бензальдегида, которые составляют соответственно 23 2; 26 4 и 44 6 кДж / моль. [39]
Юнг и другие [37] изучили реакцию натриевой соли аллилбензола в жидком аммиаке с бромистым аллилом, с хлористым а - и у-метилал-лилами и бромистым метилом, чтобы определить, включаются ли первичный и вторичный атомы углерода аллилбензола в реакцию замещения. Ими найдено, что во всех случаях присутствует продукт замещения у первичного С атома ( С Н5 - СНСН-CH2R), в некоторых преобладает продукт у вторичного С атома ( С Н6 - GHR-CHGH. [40]
Оценкой изомеризующей способности различных контактов служила степень изомеризации аллилбензола при проведении его над этими контактами. [41]
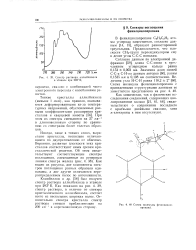 |
Спектр раствора аллилбензола в этаноле при 293 К.| Схема молекулы фенилциклопропана. [42] |
Кэмпбеллом и др. [58] был получен спектр раствора аллилбензола в этаноле при 293 К. Относительно спектра кристалла спектр раствора смещен приблизительно на 200 см в коротковолновую сторону. [43]
Аналогично может быть проведено гидрирование других непредельных соединений - аллилбензола, стирола, 1-гептена, ма-леиновой или коричной кислот и др. Катализатор Pd / CaCO3, a также другие нанесенные катализаторы следует брать в количестве 5 - 10 % от массы гидрируемого вещества. [44]
Получают магнийбромфенил, как это описано в опыте по получению аллилбензола. После окончания прибавления двуокиси углерода реакционную массу разлагают 5 % - ной соляной кислотой до образования двух прозрачных слоев. Эфирный слой отделяют, водный - экстрагируют дважды по 20 мл эфиром. После отгонки эфира остаток перекристаллизовывают из воды. [45]
Страницы: 1 2 3 4