Третичные амид
Cтраница 3
Хотя сам Фридман не опубликовал детальной методики проведения этой реакции, однако впоследствии многие исследователи с успехом применяли ее для получения различных альдегидов. Первоначально в качестве исходных веществ были использованы нитрилы и третичные амиды, из которых при действии 0 25 моля алюмогидрида лития получались альдегиды. [31]
Ни у одного из этих соединений не обнаруживается каких-либо изменений частоты СО при введении первого атома галогена. Но когда вводится второй атом галогена, то у третичных амидов появляются два пика, соответствующие поворотным изомерам, а у вторичных амидов - один пик при несколько более высокой частоте. Отсутствие поворотной изомерии у вторичных амидов объясняется Найквистом [72, 73] образованием внутримолекулярной водородной связи NH С1, которая закрепляет атом галогена в г ис-конфигу-рации относительно атома азота. Это предположение подтверждается поведением частот валентных колебаний NH. Любые дополнительные атомы галогенов будут затем занимать скошенное положение относительно атома карбонильного кислорода, при котором эффект поля уменьшится. [32]
В молекулярных ионах сложных эфиров, а также вторичных или третичных амидов перегруппировка Маклаф-ферти может осуществляться и по другому пути с участием группы X. И снова по аналогии с альдегидами и кетонами положительный заряд может локализоваться и на алкеновом фрагменте, особенно если он эффективно стабилизирован. [33]
Повышение двоесвязности атомов углерода и азота амид-ной группы обусловливает возможность поворотной изомерии. Действительно, СО - и ( Z) - изомеры вторичных и несимметрично замещенных третичных амидов при комнатной температуре существуют как индивидуальные соединения. Естественно, что в спектре смеси СО - и ( Z) - амидов представлены полосы, отвечающие обоим изомерам. [34]
Однако вторичные амиды имеют также сильную характеристическую полосу при более низких частотах, природа которой являлась предметом многочисленных дискуссий. Многие авторы относят ее к деформационным колебаниям NH, что подтверждается отсутствием такой полосы у третичных амидов. Однако возникают затруднения при объяснении отсутствия амидной полосы II у циклических лактамов, и это вызывает необходимость сделать иные предположения. [35]
Они обнаружили, что между частотами этих соединений и частотами ацетона в тех же растворителях не существует линейной зависимости, но такая зависимость имеется между смещениями частот различных третичных амидов. Это отличие третичных амидов от других карбонильных соединений обусловлено, вероятно, присутствием основного атома азота, который представляет дополнительный центр взаимодействия с растворителем. [36]
Иногда полезно заменить уксусную кислоту бензойной или трифторуксусной. Реагент, полученный с применением трифтор-уксусной кислоты, восстанавливает УУ-ацетилиндол. Третичные амиды не восстанавливаются; это указывает на то, что диборан не участвует в реакции. [37]
По отношению к большинству функциональных групп, кроме алкенов, поведение тексилборана аналогично поведению комплекса боран - ТГФ. Реакция протекает только при кипячении в ТГФ, иногда очень медленно, но выход альдегида обычно высок. Третичные амиды также медленно восстанавливаются до альдегидов, но тексилборан для этих целей используется редко, так как восстановление дисиамилбораном, по-видимому, здесь лучше. [38]
Многие реакции амидов с галогенангидридами неорганических кислот используются в органическом синтезе. Эти реагенты можно подразделить на три класса: а) фосген, тионилхлорид и пента-хлорид фосфора; б) оксихлорид фосфора и аренсульфонилхло-риды; в) фторангидриды кислот. В случае третичных амидов удается выделить некоторые относительно стабильные комплексы, однако в случае вторичных и первичных амидов происходят дальнейшие превращения, такие, как N-деалкилирование и дегидратация, быстро приводящие к нитрилам. [39]
Они обнаружили, что между частотами этих соединений и частотами ацетона в тех же растворителях не существует линейной зависимости, но такая зависимость имеется между смещениями частот различных третичных амидов. Это отличие третичных амидов от других карбонильных соединений обусловлено, вероятно, присутствием основного атома азота, который представляет дополнительный центр взаимодействия с растворителем. [40]
В ИК-спектрах первичных, вторичных и третичных амидов присутствует очень интенсивная полоса поглощения ( полоса I) в области 1650 - 1700 см-1, обусловленная валентными колебаниями С - О. Точное положение этой полосы зависит также от условий ( фазового состояния) регистрации спектра. Исключение составляют лишь третичные амиды, которые не дают ассоциатов за счет водородных связей. Как правило, частота амидной полосы I ниже, чем частота поглощения, обусловленного валентными колебаниями других карбонильных групп, например кетонов. Это обусловлено тем, что связь С-О приобретает частично односвязный характер в результате делокализации неподеленной пары электронов азота ( см. разд. Положение полосы зависит также от наличия или отсутствия заместителей у атома азота и от их электроотрицательности. [42]
По-видимому, не существует никакой корреляции между интенсивностью и частотой карбонильного поглощения или основностью карбонильных соединений. Частоты N-диалкилзамещенных соединений немного меньше соответствующих частот монозамещенных амидов: М М - диметилацетамид поглощает при 1653 см-1, a N N-диметилбензамид - при 1644 см-1. Спициел и Фримен [247] исследовали влияние замещения галогеном в а-положении у третичных амидов. Полученные результаты сходны с данными для монозамещенных соединений с той разницей, что у дизамещенных производных отсутствуют эффекты, связанные с образованием внутримолекулярной водородной связи. N-Диметилтрихлорацета - мид характеризуется vCO 1689 см-1, эта величина несколько выше, чем значение для моноалкилзамещенного соединения. [43]
Металлорганические соединения, такие как реактивы Гриньяра или литийалкилы, взаимодействуют с первичными и вторичными амидами, а также с амидами, имеющими протоны у углеродного атома, находящегося в а-положении по отношению к карбонильной группе, как сильные основания, отнимая кислые протоны. Несколько примеров, включающих такие реакции, приведены в разд. Нуклеофильное присоединение реактивов Гриньяра [247] и литийорганических соединений [248] к карбонильной группе третичных амидов представляет некоторый теоретический, хотя и незначительный, препаративный интерес. Этот процесс, вероятно, включает согласованную атаку фрагментов - атома металла и карбаниона - на атомы кислорода и углерода амида соответственно. [44]
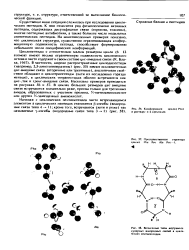 |
Конформация цикло ( Pro в растворе и в кристалле.| Пространственная структура цикло ( Phe Pro Ala Pro -.| Возможные типы внутримоле кулярных водородных связен в циклических лентапептндах. [45] |
Страницы: 1 2 3 4