Сывороточный альбумин
Cтраница 3
К первой группе относятся сывороточный альбумин и у-глобулин человека и яичный альбумин. Эти белки почти совсем не сорбируются на солевой форме смол, в то время как на водородной форме той же смолы они сорбируются со значительной емкостью. Этот результат можно интерпретировать как наличие близко расположенных в третичной структуре белков положительно и отрицательно заряженных функциональных групп. Белки этой группы не способны вступать во взаимодействие с катионитом за исключением того случая, когда возможен перенос протона с нейтрализацией карбоксильных групп белка. В отличие от этого вторая группа белков - инсулин, адренокор-тикотрошшй гормон, миоген, рибонуклеаза, химотрипсин и хи-мотрипсиноген и ряд других сорбируются с сопоставимыми емкостями на обеих формах смол. [31]
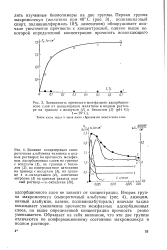
Вторая группа макромолекул ( сывороточный альбумин ( рис. 4), лизоцим, яичный альбумин, казеин, поливинилбутираль) вначале также показывает увеличение прочности межфазных адсорбционных слоев, но выше определенной концентрации прочность резко уменьшается. Обращает на себя внимание, что эти две группы отличаются по конформационному состоянию макромолекул в водном растворе. [33]
К первой группе относятся сывороточный альбумин и - у-глобулин человека и яичный альбумин. Эти белки почти совсем не сорбируются на солевой форме смол, в то время как на водородной форме той же смолы они сорбируются со значительной емкостью. Этот результат можно интерпретировать как наличие близко расположенных в третичной структуре белков положительно и отрицательно заряженных функциональных групп. Белки этой группы не способны вступать во взаимодействие с катионитом за исключением того случая, когда возможен перенос протона с нейтрализацией карбоксильных групп белка. В отличие от этого вторая группа белков - инсулин, адренокор-тикотропный гормон, миоген, рибонуклеаза, химотрипсин и хи-мотрипсиноген и ряд других сорбируются с сопоставимыми емкостями на обеих формах смол. [34]
В частности, бычий сывороточный альбумин характеризуется высоким значением А595 и поэтому не может быть использован в качестве общего стандартного белка в этой методике. [35]
Вторая группа макромолекул ( сывороточный альбумин, лизоцим, казеин, ПВБ) вначале также показывает увеличение прочности межфазных адсорбционных слоев, но выше определенной концентрации прочность слоев резко уменьшается. Обращает на себя внимание, что эти две группы отличаются по конформационному состоянию макромолекул в водном растворе. Пространственные структуры макромолекул второй группы в большей степени стабилизованы внутримолекулярными гидрофобными связями. При больших концентрациях макромолекул в растворе возникающий вначале межфазный слой составлен из макромолекул, конформация которых практически не отличается от конформации в объеме водного раствора. Высокая концентрация беспорядочных клубков ( желатина, ПВО, ПВФ) в межфазном адсорбционном слое приводит к одновременному возникновению большого числа межмолекулярных нековалейтных связей, что и является причиной образования пространственной структуры в межфазном слое. Предложенный механизм образования межфазных пространственных структур напоминает процесс объемного структурообразования ( гелеобразо-вания) в водных растворах тех же макромолекул. [36]
Примером кислых белков являются сывороточный альбумин быка, fi - лакто-глобулин; примером основных - лизоцим, цитохром С. [37]
Примером кислых белков являются сывороточный альбумин быка, [ 3-лакто-глобулин; примером основных - лизоцим, цитохром С. [38]
При анализе спектров ЭПР спин-меченого сывороточного альбумина было обнаружено, что большая часть свободных радикалов находится в таком же связанном состоянии, как и в случае поли - L - лизина. Однако в спектре можно было наблюдать еще и компоненту сигнала ЭПР с другими параметрами, которые характерны для иминоксильных радикалов в твердых органических стеклах. [39]
Стандартный раствор белка, например сывороточного альбумина, содержащий 10 мг в 1 мл. [40]
Стандартный раствор белка, например сывороточного альбумина, содержащий 1 мг в 1 мл. [41]
Для реакции иодида с сывороточным альбумином совпадение с экспериментальными данными может быть получено не меньше, чем для трех классов участков. [43]
НЬ-гемоглобин; Cyt-цитохром; BSA-бычий сывороточный альбумин. [45]
Страницы: 1 2 3 4