Дефицит - катион
Cтраница 2
Так, если в реакциях гидрирования декатионйрование приводит к получению малоактивного неселективного катализатора [35], то в реакциях изомеризации, полимеризации, дегидратации, наоборот, необходимым является дефицит катионов. Небольшая степень декатионирования позволяет резко повышать активность щелочных форм, не изменяя селективности. Этот и целый ряд других экспериментальных фактов ( отравляющее действие оснований на активность щелочных форм цеолитов [10, 11], хорошее согласие с экспериментом расчетных селективностей в реакции изомеризации бутенов в случае предположения карбо-ний-ионного механизма [1, 2]) говорят в пользу кислотной природы активности щелочных форм в реакциях карбоний-ионного типа, тем более что эти реакции протекают на щелочных формах с образованием продуктов, типичных для кислотных катализаторов. [16]
Полученные нами экспериментальные данные, включающие и исследование декатионированных форм этих образцов в реакции, а также изучение адсорбции основания методом ИКС позволили установить, что активность щелочных форм цеолитов в реакции изомеризации гексана-1 обусловлена наличием на их поверхности небольшого количества слабых кислотных центров, которые могут являться результатом дефицита катионов. [17]
Сопоставление активности цеолитов У в образовании бутена-1 показывает, что рост дефицита катионов приводит к увеличению активности. Дефицит катионов в структуре цеолита приводит к проявлению протоно-донорных свойств. [18]
Пропилен превращается в продукты уплотнения на 92 %, а гидрирование пропилена очень незначительно. Отсюда можно сделать вывод о том, что дефицит катионов натрия в исходных натриевых цеолитах, также являющийся причиной появления кислотных свойств у цеолитов [25, 27], будет ухудшать селективность. [19]
В спектрах цеолита NaX полосы при 3750, 3695 и 3655 см-1 действительно удалось наблюдать, однако те же полосы появились и в спектре, полученном на тонких, тщательно отмытых или обработанных разбавленной соляной кислотой таблетках. В результате был сделан вывод, что присутствие небольшого числа структурных гидроксильных групп можно объяснить дефицитом катионов или наличием примесей в цеолитах. Таким образом, удастся или не удастся обнаружить полосы гидроксильных групп, видимо, зависит от степени дефицита катионов и чувствительности спектральной аппаратуры. [20]
К-формы или смешанные Na, К-формы цеолитов неактивны в большинстве превращений углеводородов по карбониево-ионному механизму. Однако Холл и Ломбарде [169-171] показали, что в этих случаях появление активных центров обусловлено дефицитом катионов из-за небольшого числа протонов, вводимых в цеолиты при промывке водой, или же присутствием следов многозарядных катионов ( Са2), а сам по себе цеолит NaY, судя по ИК-спектрам дегидратированных образцов [172] или по результатам титрования [83], не обладает кислотностью. Между тем известно, что в реакциях превращения углеводородов цеолиты с обменными двузарядными катионами становятся активными, как правило, только после того, как катионы заполнят большую часть мест Sj. Поэтому вопрос о том, каким образом небольшое число катионов Са2, лока - - лизованных в местах Sb может вызвать сдвиг двойной связи, остается неясным. Холл и соавторы считают, что Н2О, возможно, выполняет роль сокатализатора, меняя распределение катионов. [21]
Важнейшей причиной часто наблюдающихся расхождений результатов измерений тештот адсорбции является, по-видимому, неполная идентичность образцов, используемых разными авторами. Небольшие различия в содержании катионов разной природы, наличие сверхстехиометрических щелочей или, напротив, некоторого дефицита катионов, возникающего обычно при отмывке, примеси, а также различия в числе катионов в элементарной ячейке цеолита, обусловленные разницей отношений Si / Al в решетке изучавшихся образцов, могут привести к существенным изменениям теплот адсорбции. Даже образцы цеолитов одного и того же структурного типа и очень близкого химического состава могут различаться по своим адсорбционным свойствам. Это связано с неидентичностью условий синтеза [19-21], структурно-химического модифицирования [23-25] и термообработки [26-32] разных образцов. [22]
Их активность в реакции дегидратации авторы [12-14] связывают с дефицитом катионов натрия, отмечая при этом корреляцию между активностью и силовым полем катиона. Авторы [15-16] предполагают, что в реакции дегидратации метанола активны два типа центров - электроноакцепторные и про-тонодонорные, обусловленные дефицитом катионов. [23]
Во-вторых, сумма обменных катионов, определенная по данным химического анализа, оказалась ниже максимальной обменной емкости этих цеолитов, т.е. имеет место дефицит катионов в твердой фазе. Исходя из этого можно предположить, что двухвалентные катионы входят в цеолиты в частично или полностью гидратирован-ном состоянии, а наблюдающийся дефицит катионов, вероятно, связан либо с понижением заряда матрицы цеолита за счет внедрения протона в алюмокремнекислородные тетраэдры с образованием ОН - - группы, либо с образованием иона оксония ( Н3О) в результате взаимодействия протона с цеолитной водой, который в этом случае становится третьим конкурирующим катионом в ионообменной системе. [24]
Для NH3 на декатионированных образцах, в отличие от С02, имеет место взаимодействие хемосорбционного типа. Некоторое снижение адсорбции NH3, наблюдавшееся при де-атамшшровании ( см. изотермы 2 и 3, рис. 2, б), связано, вероятно, с уменьшением числа кислотных центров ( если отождествлять их с дефицитом катионов) в деалюминированном образце. Кроме того, сами хемосорбирован-ные молекулы аммиака и образовавшиеся ионы аммония, по-видимому, являются своего рода вторичными центрами адсорбции. Поскольку суммарное число этих центров и катионов в деалюминированном образце меньше, чем в декатионированном, то это может являться другой причиной наблюдающегося снижения адсорбции NH3 при деалюминировании. [25]
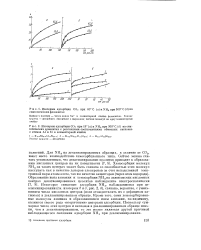 |
Изотермы адсорбции С02 при 60 С ( а и NH3 при 300 С ( б на синтетических фожазитах. [26] |
Для NH3 на декатионированных образцах, в отличие от С02, имеет место взаимодействие хемосорбционного типа. Образование иона аммония и хемосорбция NH3 на льюисовских кислотных центрах декатионированных цеолитов наблюдались спектроскопически [7 8] Некоторое снижение адсорбции NH3, наблюдавшееся при де-ал юминировании ( см. изотермы 2 и 3, рис. 2, б), связано, вероятно, с уменьшением числа кислотных центров ( если отождествлять их с дефицитом катионов) в деалгомшшрованном образце. Кроме того, сами хемосорбирован-ные молекулы аммиака и образовавшиеся ионы аммония, по-видимому, являются своего рода вторичными центрами адсорбции. Поскольку суммарное число этих центров и катионов в деалюминированном образце меньше чем в декатионированном, то это может являться другой причиной наблюдающегося снижения адсорбции NH3 при деалюминировании. [27]
Дефицит катионов или наличие примесей приводит к появлению кислотности. Кислотные свойства этих образцов, как, впрочем, и других исследованных цеолитов, связаны с присутствием бренстедовских, а иногда и льюисовских центров, соотношение между которыми зависит от температуры термической обработки. Прогревание цеолитов при температурах ниже 450 С способствует образованию главным образом бренстедовских кислотных центров, а прогревание при температурах выше 600 С благоприятно для формирования льюисовских центров. Повышение температуры прогревания цеолитов меняет соотношение центров в сторону усиления льюисовской кислотности, тогда как при добавлении воды число льюисовских центров уменьшается. Бренстедовские кислотные центры цеолитов с многозарядными катионами и декатионированных цеолитов по своей природе одинаковы и, вероятно, представляют собой гидроксильные группы с частотой колебаний 3650 и 3550 см - Этим двум полосам отвечают центры с различной силой кислотности и, возможно, с различной локализацией в структуре. Близкими между собой оказались и льюисовские кислотные центры, связанные с существованием трех-координированных атомов алюминия, которые образуются при дегидроксилировании. [28]
В результате при отношении катиона к алюминию, равном 1, фактически будет наблюдаться дефицит катионов. После того как степень обмена натрия, первоначально содержащегося в цеолите, достигает 75 %, оставшиеся катионы натрия и протоны могут быть замещены только на те редкоземельные катионы, которые проявляют наибольшую избирательность при обмене. В этом случае дефицит катионов достигает минимума и из ИК-спек-тра исчезает высокочастотная полоса поглощения. [29]
Я думаю, что, выбирая ион кислорода, к которому наиболее вероятно присоединение протона в цеолитах типов X и Y, не следует ограничиваться только двумя типами ионов, имеющихся в шестичленных кислородных кольцах, но нужно рассмотреть также и другие два типа, и особенно ионы, образующие мостики между содалитовыми ячейками. Именно около них нет соседних цеолитных катионов, они имеют искаженный угол между связями, вследствие чего возможность образования водородной связи с соседними ионами кислорода достаточно велика. Я не утверждаю, что ионы кислорода на шестичлеппых кольцах с дефицитом катиона не могут присоединять протон; я только указываю на другую возможность. Конечно, катионы металлов предпочитают шестичленные кольца, где они лучше стабилизированы и электрически экранированы. [30]
Страницы: 1 2 3