Дихлоргидрин
Cтраница 1
Дихлоргидрин, перегоняющийся в пределах указанных семи градусов, достаточно чист для большинства целей. Он почти не содержит изомерного дихлоргидрина, так как при окислении дает хорошие выходы соответственного дихлорацетона ( стр. [1]
Дихлоргидрин лучше всего получать не аналогично этиленхлоргидрину ( см. стр. Реакция хлористого аллила с хлорноватистой кислотой протекает в водном растворе; контакта между свободным хлором и хлористым аллилом нужно избегать, иначе произойдет присоединение хлора. Источником хлорноватистой кислоты служит гипохлорит натрия, на который действуют хлором. [2]
Дихлоргидрин можно также гидролизовать непосредственно в глицерин в одну стадию. Затем 5 % - ный водный раствор глицерина упаривают в вакууме до концентрации 80 %, освобождают от соли, дополнительно упаривают до 98 % и удаляют выделившуюся соль. Обессоленный концентрат глицерина обесцвечивают обработкой углеводородным растворителем. В заключение глицерин очищают перегонкой с водяным паром в вакууме. Полученный продукт содержит не менее 99 % глицерина и отвечает требованиям фармакопеи США. [3]
Дихлоргидрин состоит из смеси сс р - и а у-изомеров, представляющих собой жидкости, ограниченно растворимые в воде. [4]
Дихлоргидрин и продукты его окисления. [5]
Дегидрохлорирование дихлоргидрина также приводит к образованию эпихлоргидрина. Непрерывный способ его получения состоит в том, что хлор взаимодействует с аллилхлоридом в водной среде с образованием солянокислого раствора глице-риндихлоргидрйна, который нейтрализуют раствором СаСО3 или Са ( ОН) 2 и омыляют добавлением Са ( ОН) 2; из полученного раствора выделяют Эпихлоргидрин. В качестве щелочного агента рекомендуют порошкообразный Са ( ОН) 2, содержащий 2 - 8 % MgO. Смесь дихлоргидринов глицерина смешивают в реакторе с 10 % - и водной суспензией Са ( ОН) 2 и MgO при 40 С, поддерживая время контакта 5 мин. Отгоняют азеот-роп вода - Эпихлоргидрин при 94 С. Водный слой, содержащий 5 % эпихлоргидрина, возвращают в колонну. Сырой эпихлоргид-рин содержит 90 % целевого продукта ( Пат. Предлагается способ получения эпихлоргидрина из сбросовых вод реактора получения эпихлоргидрина ( А. [6]
Выход дихлоргидрина зависит от температуры в зоне реакции. В результате основной и побочных реакций раствор дихлоргидрина нагревается на 18 - 20 С. Если исходный раствор НОС1 поступает с температурой 18 - 20 С, то получаемый раствор дихлоргидрина нагревается до 35 - 38 С. Это предельная температура, выше нее скорость побочных реакций увеличивается и выход дихлоргидрина снижается. Целесообразно проводить реакцию с отводом тепла, чтобы температура была 20 - 30 С. [7]
Синтез дихлоргидрина метриола и этриола и их моноэфиров заключается в гидрохлорировании метриола и этриола при повышенной температуре в среде органической кислоты в условиях, обеспечивающих вынос воды, образующейся при реакции. [8]
Для получения дихлоргидрина аллихлорид вводят в реакцию обмена с хлорноватистой кислотой в водной фазе. Поскольку аллилхлорид плохо растворяется в воде ( при 20 С в воде растворяется только 0 36 вес. В противном случае в результате присоединения хлора образуется слишком большое количество трихлорпропана. [9]
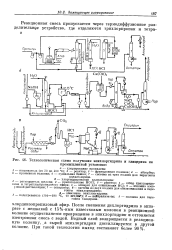 |
Технологическая схема получения эпихлоргидрина и глицерина на. [10] |
После смешения дихлоргидрина в аппарате с мешалкой с 15 % - ным известковым молоком в реакционной колонне осуществляется превращение в эпихлоргидрин и отгоняется азеотропная смесь с водой. [11]
Незначительный унос дихлоргидрина с парами из реакционной зоны объясняется тем, что он образует с водой азеотропную смесь ( 92 % дихлоргидрина и 8 % воды), кипящую при 93 С. [12]
Преимущество метода дихлоргидринов состоит в том, что если не выделять эпихлоргидрин, то можно прямо перейти к получению глицерина. Кроме того, при необходимости этим методом можно получать эпихлоргидрин. [13]
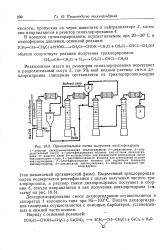 |
Принципиальная схема получения эпихлоргидрина. [14] |
Дегидрохлорирование смеси дихлоргидринов осуществляется в аппаратах 1 колонного типа при 95 - 103 С. Подача дихлоргидринов глицерина осуществляется с помощью барботеров, установленных в нижней части колонн. [15]
Страницы: 1 2 3 4