Использование - уравнение - состояние
Cтраница 2
При использовании уравнения состояния для моделирования фазового равновесия и теплофизических свойств многокомпонентной системы необходимы следующие данные, характеризующие эту смесь: мольный компонентный состав; свойства каждого компонента - критические давление и температура, ацентрический фактор; коэффициенты бинарного взаимодействия компонентов. [16]
При использовании уравнения состояния Пента - Робинсона ( ПР) плотность смеси находится в процессе решения самого уравнения. Как показано в [30], погрешность вычисления плотности газовых смесей ло уравнению состояния ПР не превышает 1 5 % в диапазоне давлений и температур, встречаемых в промысловой практике. Содержание суммы кислых компонентов в смеси может доходить до 50 мол. [17]
При использовании уравнения состояния идеального газа ( PV RT для 1 моля газа) отклонение реальной системы от идеальной при давлении выше 10 МПа может составлять несколько десятков или сотен процентов. [18]
Рассмотрим некоторые вопросы использования уравнений состояния и пробегов фотонов в газодинамических расчетах. Необходимые теплофизические данные, как правило, хранят в виде таблиц, которые можно легко модифицировать и уточнять по мере необходимости. Подробность используемых в таблицах сеток определяется требованием передачи особенностей поведения физических величин, при этом наиболее экономичными обычно оказываются неравномерные сетки, в частности, по температуре и плотности. Полученные табличные данные используются в дальнейшем на более подробных сетках, определяемых методами численного решения задач радиационной газовой динамики. Это обуславливает необходимость многократной интерполяции таблично заданной информации. [20]
В качестве примера использования уравнений состояния (2.4) дадим решение плоской задачи о действии давления q ( x, t) на неоднородно-стареющий вязкоупругий тонкий1) слой ( Ы, O y h), лежащий без трения на жестком основании. [21]
В качестве примера использования уравнений состояния (2.11) рассмотрим, как и выше, плоскую задачу о действии давления q ( x, t) на нелинейно-стареющий вязкоупругий тонкий слой ( Ы 0, 0 yh), лежащий без трения на жестком основании. [22]
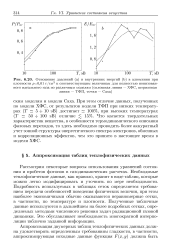
Заключение о возможности использования уравнения состояния идеального газа было сделано Вант-Гоффом после того, как полученные значения я / с для растворов сахара оказались очень близкими к значению газовой постоянной. Однако для многих растворов уравнение (6.1) дает большое расхождение с экспериментальными данными ( рис. 6 - 1), особенно при высоких температурах. [23]
Результаты расчетов с использованием уравнения состояния Ван-дер - Ваальса отличаются низкой степенью точности, особенно вблизи критического состояния газов. Тем не менее, уравнение (6.1) является полезным приближением и служит основой для построения обобщенных диаграмм сжимаемости. [24]
Метод основан на использовании уравнения состояния РК - Содержание углекислого газа и сероводорода в смеси учитывается при вычислении критических параметров ее компонентов, методика расчета которых состоит в следующем. [25]
Более полный расчет требует использования уравнения состояния, которое для бинарных систем при высоких значениях параметров неизвестно. Так, по Креглевскому, газовый раствор рассматривается как регулярный раствор. [26]
Следует отметить, что использование уравнений состояния для реальных газов в обычных инженерных расчетах наталкивается на значительные трудности, связанные и с невысокой точностью и большой затратой времени. [27]
Оно выведено на основании использования уравнения состояния для газа, в частности, применения уравнения Пуассона для адиабатического процесса и связи универсальной газовой постоянной с удельными тешюемко-стями Ср и Су. Эта соображения для жидкости неприменимы, более того, для жидкости отсутствует выражение, аналогичное уравнению состояния. [28]
Расчет фазового равновесия с использованием уравнений состояния основан на строгом применении классических положений термодинамики многокомпонентных систем - равенстве химических потенциалов ( ле-тучестей) компонента смеси во всех сосуществующих фазах. [29]
Таким образом, при использовании уравнений состояния для многокомпонентных систем важнейшим моментом является то, по каким правилам вычисляются коэффициенты уравнения состояния. [30]
Страницы: 1 2 3 4