Амидокислота
Cтраница 3
Эпоксидирование амидокислот практически не изучено. Нами показано, что амидолактон 5 образуется при эпоксидировании амидокислоты 4 ( продукта амино-лиза эндикового ангидрида) трифторпероксиуксусной кислотой в момент ее образования из трифторуксусного ангидрида и 50 % - ного раствора пероксида водорода. Амидолактон 5 идентичен полученному ранее по вышеприведенной схеме. [31]
Смотря по тому, который из водородных атомов фенила в бензойной кислоте замещается аммиакальным остатком H N, должна получиться или амидобензойная, или амидодрациловая, или антраниловая кислота ( ср. При восстановлении образующейся прямым нитрованием нитробензойной кислоты получается, как известно, первая из названных амидокислот. В настоящее время сделался известным путь, которым переходят от бензойной кислоты к кислоте антраниловой. Бро-мированием бензойной кислоты получают одну однобромбензойную кислоту: но последняя, подвергаясь нитрованию, дает две изомерные бромни-тробензойные кислоты, которые, в свой черед, при восстановлении дают две изомерные однообромленные амидобензойные кислоты. [32]
Интересно рассмотреть поведение солей в присутствии ПМДА. На кривой титрования моносоли ( рис. 4) раствором ПМДА наблюдается скачок потенциала, и хотя он плохо выражен, но количественно соответствует взаимодействию моносоли с ПМДА с образованием амидокислоты и выделением свободной ПМК. [33]
При расчете элементарного состава предполагалось, что исходная пленка заимидизована на 100 % и что при деструкции отщепляются группы СО только имидных циклов. Примерно такие же расчетные данные элементарного состава получаются, если предполагать, что исходная пленка содержит 80 % имидных и 20 % амидокислотных звеньев по весу и что при деструкции имид разлагается с выделением четырех молекул СО на каждое звено, а амидокислота - по термогидролитическому механизму по выше приведенной схеме. С предположениями, сделанными при расчете, хорошо согласуется тот факт, что остаток образца обогащается азотом и в нем резко снижается содержание кислорода. [34]
При нагревании с метиловым спиртом под давлением имиды алифатических кислот разлагаются, причем образуются эфиры амидокислот. Реакцию проводят 35 ч в запаянной трубке с 8-кратным количеством абсолютного метилового спирта при температуре 170 С. Эфиры амидокислот перекристаллизовывают из ацетона 4, Реакция неприменима к имидам ароматического ряда. [35]
Амиды кислот так же, как и карбоновые кислоты, образуют ассо-циаты даже в растворе органических растворителей. Молекулы амидокислот имеют ярко выраженную ди-польную структуру, причем величина дипольного момента в них выше, чем можно было ожидать, принимая во внимание только несимметричное строение молекулы. [36]
Несколько более далеки от природных жиров соли амидов кислот. Амидные группы, связывая молекулы соли водородными связями, приводят к образованию кристаллитов и могут способствовать повышению температуры плавления, загущающей способности, стабильности при перемешивании и водостойкости консистентных смазок. Потенциальные преимущества амидокислот первоначально не удалось полностью реализовать, так как применявшийся метод их приготовления приводил к образованию смесей, в которых присутствовали некоторые низкоплавкие и слабозагущающие компоненты, например диамидокислоты, не содержавшие солевых групп. [37]
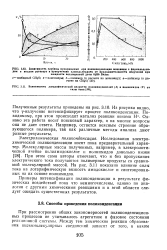
При этом сами авторы отмечают, что и без пропускания электрического тока получаются полимерные продукты со сравнимой молекулярной массой. На рис. 3.11 показано влияние силы тока на логарифмическую вязкость амидокислот и синтезированных на их основе полиимидов. [39]
Отношение к различным источникам азота у микроорганизмов довольно специфично. Они могут использовать азот из самых различных источников. Так, бактерии способны усваивать азот из сложных белковых веществ, простых растворимых белков, из азотнокислых и аммиачных солей, а также потребляют аммиак и свободный азот атмосферы. Для дрожжей лучшим азотистым питанием является водный раствор аммиака и аммиачные соли, аминокислоты, амидокислоты и мочевина, хуже усваивается пептон. Источником кислорода и водорода является в основном вода. [40]
Подобно аминокислотам, амидокислоты во многих случаях имеют в этой области широкие и довольно слабые полосы поглощения. Проведенный Фасоном и др. [18] анализ опубликованных данных показывает, что полоса поглощения в интервале 2640 - 2360 см 1 наблюдается для 23 соединений из 26, а другая полоса в интервале 1945 - 1835 слГ1 наблюдается для 16 из 26 соединений. Эти полосы являются иногда сложными и, вероятно, составными; они наблюдаются не всегда, что уменьшает их значение. При интерпретации спектров неизвестных веществ надо помнить, что в этой области, кроме аминокислот и их гидрохлоридов, могут поглощать также и амидокислоты. Это, вероятно, характеристическое поглощение карбоновых кислот, соответствующее поглощению вблизи 2650 см 1, которое наблюдается у димеров карбоновых кислот ( гл. [41]
Подобно аминокислотам, амидокислоты во многих случаях имеют в области 3000 - 2000 см 1 широкие и довольно слабые полосы поглощения. Проведенный Фасоном и др. [18] анализ опубликованных данных показывает, что полоса поглощения в интервале 2640 - 2360 см-1 наблюдается для 23 соединений из 26, а другая полоса в интервале 1945 - 1835 см-1 наблюдается для 16 из 26 соединений. Эти полосы являются, вероятно, составными; они наблюдаются не всегда, что уменьшает их значение. При интерпретации спектров неизвестных веществ важно помнить, что в этой области, кроме аминокислот и их гидрохлоридов, могут поглощать также и амидокислоты. [42]
Но следует подчеркнуть факт появления первых идей о пептидном строении белков в трудах А. Я. Данилевского, из которых приведу следующие принципиальные высказывания [259]: В нормальном организме азот амидокислотной группы появляется в форме мочевины, мочевой кислоты, так точно, как и весь остальной азот частицы. Уже и первом моем сообщении я приводил факты, показывающие, что появление аминокислот при распаде белков всегда сопровождается разрушением биуретовой группы. Вообще существуют веские основания принимать, что амидокислотные группы находятся в частице не только в непосредственной связи с биуретовой группой, по что их азот в такой же мере принадлежит им, как и биуретовой группе. Другими словами я принимаю, что обе эти группы связаны между собою атомом азота, который, составляя неотъемлемую часть биуретовой группы при целости белковой частицы, может при ее распаде стать азотом появляющейся амидокислоты. Это положение так важно для дальнейшего изучения конституции, что необходимо принести в пользу его все имеющиеся на лицо фактические доказательства ( стр. Далее приводится длинный ряд убедительных доводов в пользу тезиса, что в белковой частице углеазотная группа не есть собственно остаток биурета, но она есть комплекс атомов CuN, способных интрамолскулярно стать во взаимное отношение, как в биурете. В цитированной работе А. Я. Данилевский многократно возвращается к вопросу о характере связи различных остатков белковой молекулы друг с другом и высказывает твердое убеждение о - СО-NH - типе этой связи, известной сейчас под названием пептидной связи. [43]
Кроме того, нахождение других замещающих функциональных групп в непосредственной близости от амидной группировки часто приводит к заметным изменениям в спектре. Например, спектры соединений, содержащих структурную группу СО - NH - СО, настолько отличаются от спектров нормальных амидов, что их можно дифференцировать. Уретаны и анилиды более сходны с нормальными амидами, но у замещенных мочевины интерпретация области 1600 см 1 становится чрезвычайно затруднительной из-за сложности полос поглощения NH. Однако, согласно имеющимся данным, полоса карбонильного поглощения амида имеет обычную частоту. Амидокислоты рассматриваются в гл. [44]
Страницы: 1 2 3