Диэтилдитиокарбамината
Cтраница 2
Нерастворимый в воде Диэтилдитиокарбаминат кобальта экстрагируется четыреххлористым углеродом и другими органическими растворителями. Фотометрическое определение основано на измерении оптической плотности неводного экстракта. Для определения кобальта в присутствии посторонних элементов предложено два метода, один из которых основан на одновременном извлечении диэтилдитиокарбаминатов нескольких металлов в неводную фазу и измерении светопоглощения при различных длинах волн, а второй - на применении маскирующих средств. [16]
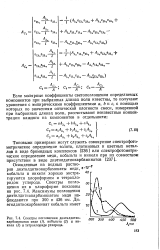 |
Спектры поглощения диэтилдитиокарбаминатов меди ( 1, кобальта ( 2 и ни-келя ( 3 в тетрахлориде углерода. [17] |
Осажденные из водных раство-ров диэтилдитиокарбаминаты меди, кобальта и никеля хорошо экстрагируются хлороформом и тетрахло-ридом углерода. Спектры погло-щения их в хлороформе показаны на рис. 7.4. Максимумы поглощения диэтилдитиокарбаминатом меди на-фшдаются при 300 и 436 нм. [18]
Первые, например 8-оксихи-нолинаты, 8-меркаптохинолинаты, диэтилдитиокарбаминаты, ди-тизонаты, купферонаты и другие, соосаждаются с индифферентными органическими соосадителями. Вторые нуждаются во введении солей тяжелых органических катионов. После этого они соосаждаются с осадками солей этих катионов с избытком примененного растворимого органического реагента непосредственно или также после добавления индифферентных соосадителей. [19]
Раствор диэтилдитиокарбамината серебра: 1 0 г диэтилдитиокарбамината серебра растворяют в химически чистом пиридине до объема 200 мл. В темном месте раствор может храниться в течение нескольких недель. [20]
Измеряя оптическую плотность хлороформного раствора, содержащего диэтилдитиокарбаминаты кобальта и никеля, можно определить концентрацию этих элементов в исследуемом растворе. Ряд тяжелых металлов ( Fe, Ti, Al, Mn, Cd, Zn и др.) мешает определению кобальта и никеля этим способом. Используя подходящие условия и применяя дополнительные комплексообразователи, можно устранить влияние некоторых катионов ( Fe, Mn Ti и др.) - Этот метод является особенно подходящим при совместном определении микрограммовых количеств Со, Ni ( и Си) в присутствии значительных количеств некоторых других металлов. [21]
Измеряя оптическую плотность хлороформного раствора, содержащего диэтилдитиокарбаминаты кобальта и никеля, можно определить концентрацию этих элементов в исследуемом растворе. Ряд тяжелых металлов ( Fe, Ti, Al, Mn, Cd, Zn и др.) мешает определению кобальта и никеля этим способом. Этот метод является особенно подходящим при совместном определении микрограммовых количеств Со, Ni ( и Си) в присутствии значительных количеств некоторых других металлов. [22]
Этот метод основан на взаимодействии тприс - ( диэтилдитиокарбамината) мышь-яка ( Ш) ( получаемого при экстракционном отделении мышьяка от других элементов) с однозамещенным дитизонатом серебра с образованием смешанного комплекса мышьяка ( Ш) с диэтилдитио-карбаминатом и дитизоном и одновременным образованием ди-этилдитиокарбамината серебра с освобождением эквивалентного количества дитизона. Концентрация выделившегося свободного дитизона пропорциональна содержанию мышьяка. [23]
Для приготовления диэтилдитиокарбамината серебра растворяют 2 25 г диэтилдитиокарбамината натрия в 100 мл воды, добавляют раствор 1 70 г нитрата серебра в 100 мл воды. Выпавший осадок диэтилдитиокарбамината серебра промывают несколько раз водой декантацией до полного удаления Ag ( I), отфильтровывают с отсасыванием и сушат в вакуум-экснкаторе. [24]
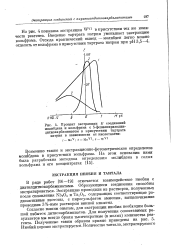 |
Процент экстракции Е соединений. [25] |
В ряде работ [16-19] отмечается взаимодействие ниобия с диэтилдитиокарбаминатами. Образующиеся соединения способны экстрагироваться. [26]
В соответствии с правилом рядов растворимости катионы, образующие менее растворимые Диэтилдитиокарбаминаты, вытесняют катионы с большей растворимостью диэтилдитиокарбаминатов. [27]
В соответ-ствии с правилом рядов растворимости катионы, образующие менее растворимые Диэтилдитиокарбаминаты, вытесняют катионы с большей раствори-мостью диэтилдитиокарбаминатов. [28]
Так, если сливать концентрированные водные растворы молибдата аммония и диэтилдитиокарбамината натрия в нейтральной или слабокислой среде, то преимущественно получается желтая форма. [29]
Метод основан на определении кадмия с дигпзоном I1J после экстракции его диэтилдитиокарбамината. [30]
Страницы: 1 2 3 4