Диэтилмагний
Cтраница 2
По данным Хорнбейкера и Конрада [847], дифенилсиландиол вступает в реакцию с диэтилмагнием или диэтилцинком, причем образуются растворимые полимеры металласилоксанового характера. Однако полученные белые порошкообразные продукты не обладают достаточной стойкостью. Полимер, содержащий магний и отвечающий по составу формуле ( C6H5) 2SiO ( MgO) 1 ] 8, pacna дается при нагревании с образованием гексафенилциклотрисил океана и окиси магния. [16]
По электропроводности можно заключить, что бромистый магний является кислотой Лыоиса, а диэтилмагний, по-видимому, может действовать как основание Льюиса. Так как комплекс должен быть более устойчивым и менее реакционноспособным, чем несвязанный диэтилмагний, его образование служит объяснением тому, что реакция гек-сина-1 с диэтилмагнием протекает примерно в 3 раза быстрее, чем с реактивом Гриньяра в сравнимых условиях. [17]
На основании свойств полученного из этилиодида белого твердого воспламеняющегося вещества ему приписывалась структура диэтилмагния; в настоящее время, по-видимому, следует считать, что это соединение отвечает этил-магнийиодиду. [18]
К эфирному раствору литийалюминийгидрида, содержащему 0 296 г литиевой соли, добавляют по каплям при постоянном помешивании раствор 2 25 г диэтилмагния в 50 мл эфира при комнатной температуре. Очень мелкий белый порошок со слабым серым окрашиванием содержит согласно анализу гидрид магния в количестве до 75 % от общего веса. Примесями в продукте являются эфир ( до 14 %), алюминий ( вероятно, в виде гидрида алюминия) и этиловый радикал. [19]
Наиболее убедительным доводом в пользу того, что реагент следует рассматривать как сольватированный комплекс R2Mg - MgX2, являются данные по ЯМР-спектрам растворов диэтилмагния и реактива Гриньяра, этилмагнийбромида, в эфире при той же концентрации. [20]
Наиболее убедительным доводом в пользу того, что реагент следует рассматривать как сольватированный комплекс R2Mg - MgX2, являются данные по ЯМР-спектрам растворов диэтилмагния и реактива Гриньяра, этилмагнийбромида, в эфире при той же концентрации. [21]
Подтверждением такого представления являются данные Ловессона и Янга, показавших, что бромид магния с дибензоил-перекисью в циклогексене образует транс-1 2-дибромциклогек-сан с выходом 83 %, а диэтилмагний с дибензоилперекисью дает этилбензоат. [22]
Интересно влияние конфигурации окиси на выход спирта при реакции с магнийорганическими соединениями. Так, из диэтилмагния и 2 3-эпокси-бутана выход З - метилпентанола-2 значительно выше в случае цис-окнси II ( см. стр. [23]
Это белые твердые, нелетучие, на воздухе окисляющиеся с воспламенением вещества. Далее отмечается, что диэтилмагний на воздухе воспламеняется легче, чем диметилмагний. [24]
Первая реакция идет в эфирном растворе. При добавке алю-могидрида к диэтилмагнию выпадает осадок, который промывают эфиром и сушат в вакууме. Полученный продукт не является чистым и содержит примесь алюминия и этильных групп, а также растворителя. [25]
Через 43 часа 33 % диэтилмагния превращается в н-бутилмагний, 2 8 % - в гексилмагний, 2 5 % - в винилмагний, 2 5 % - в гидрид магния и 13 % - в этинилмагний. В среде гексана и гептана диэтилмагний с этиленом при 100 С и 42 - 63 am образует углеводороды, содержащие 10 и более атомов углерода в молекуле. [26]
Диэтилмагний получается сходным образом. Как дифенилмагний, так и диэтилмагний ( вопреки данным более ранних исследователей) растворимы во всех отношениях в эфире. [27]
Через 43 часа 33 % диэтилмагния превращается в н-бутилмагний, 2 8 % - в гексилмагний, 2 5 % - в винилмагний, 2 5 % - в гидрид магния и 13 % - в этинилмагний. В среде гексана и гептана диэтилмагний с этиленом при 100 С и 42 - 63 am образует углеводороды, содержащие 10 и более атомов углерода в молекуле. [28]
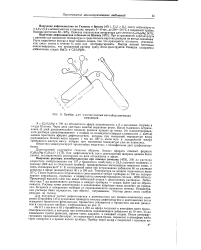 |
Прибор для очистки полных магнийорганических соединений. [29] |
Диэтилмагний получается сходным образом. Как дифенилмагний, так и диэтилмагний ( вопреки данным более ранних исследователей) растворимы во всех отношениях в эфире. [30]
Страницы: 1 2 3