Исследование - кинетика - процесс
Cтраница 2
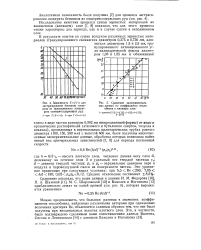
Исследование кинетики процесса выпаривания жидкостей сводится к установлению зависимости тепло - и массопередачи от определяющих факторов. [16]
Исследование кинетики процесса пароводяной коррозии показало, что наиболее совершенными защитными свойствами обладает слой магнетита. Коэффициенты линейного расширения данного окисла и стали различны и составляет соответственно 8 46 - Ог С-1 и 12 10 - 6 С-1, что является одной из причин непрочного сцепления Fe3O4 со сталью. При наличии на поверхности стали даже сплошного слоя магнетита процесс окисления при высоких температурах может продолжаться. Рост окисла в этом случае происходит преимущественно с внешней стороны, за счет диффузии ион-атомов металла к ионизированным атомам кислорода в паре, а не наоборот. При этом необходимое количество ионов кислорода поставляется молекулами водяного пара по различным промежуточным ступеням. Наиболее медленной ( контролирующей) стадией процесса окисления стали паром является диффузия ион-атомов железа через окисный слой. [17]
Исследования кинетики процессов взаимодействия металла с окружающей средой при сварке являются достаточно сложными, в связи с чем ряд вопросов не изучен и количественные зависимости не установлены. И хотя это не позволяет учитывать их количественно ( расчетом) при выборе и разработке сварочных материалов, но знание общих закономерностей позволяет сокращать объем проводимых экспериментальных проверок. [18]
Исследование кинетики процесса распада МОС при различных температурах позволяет определить температурную зависимость константы скорости реакции и выбрать наиболее подходящие температуры для осаждения пленок. [19]
Исследования кинетики процесса окисления углерода и хрома показали, что на границе пузырька и металла имеет место изменение концентрации элементов. Когда в металле остается 0 1 % С и 5 % Сг, система оказывается очень близкой к равновесной и скорость окисления углерода должна стать совсем низкой. При поступлении газообразного кислорода с той же скоростью начинается преимущественное окисление хрома. [20]
Исследование кинетики процесса вспенивания пеностекла ( рис. 3.12 и 3.13) показало, что изменение состава атмосферы, в которой протекает процесс термообработки пенообразую-щей смеси, приводит к изменению скорости процесса вспенивания пеностекла. [21]
Исследование кинетики процесса выпаривания жидкостей сводится к установлению зависимости тепло - и маесопередачи от определяющих факторов. [22]
Исследования кинетики процесса синтеза аммиака дозволяют определить энергию активации - важную характеристику каждой химической реакции. [23]
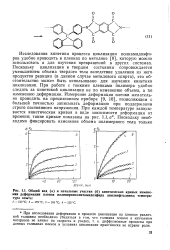 |
Общий вид ( а и начальные участки ( б кинетических кривых изменения деформации пленок полипиромеллитамидоэфира анилинфталеина. температура опыта. [24] |
Исследования кинетики процесса циклизации полиамидоэфи-ров удобно проводить в пленках по методике [8], которую можно использовать и для изучения превращений в других системах. Поскольку циклизация в твердом состоянии сопровождается уменьшением объема твердого тела вследствие удаления из него продуктов реакции ( в данном случае метилового спирта), это обстоятельство может быть использовано для изучения кинетики циклизации. При работе с тонкими пленками полимера удобно следить за кинетикой циклизации не по изменению объема, а по изменению деформации. Измерение деформации пленки желательно проводить на прецизионном приборе [9, 10], позволяющем с большей точностью записывать деформацию при поддержании строго постоянного напряжения. [25]
Исследование кинетики процесса сушки зернистых материалов во взвешенном ( кипящем) слое [7, 8] показало, что для этого процесса также характерны два периода, как и в случае сушки в неподвижном слое. [27]
Исследование кинетики процесса углекислотного окисления фосфора позволило высказать соображения о механизме реакции [48], которые, по нашему мнению, представляют известный интерес. Однако по-прежнему для выяснения механизма реакции окисления необходимы дальнейшие глубокие исследования этого процесса, так как система Р4 - С02 - Р4О10 - СО чрезвычайно сложна. Эммет и Шульц [48] остановили свое внимание лишь на последней стадии окисления, а именно на окислении четырехокиси фосфора в пяти-окись. Их наблюдения позволили высказать предположение о том, что окисление протекает с участием четырехокиси в виде димера Р204, а химическая сущность начальных стадий реакции ими не была освещена. [28]
Исследование кинетики процесса самопроизвольного диспергирования монокристаллов олова в присутствии сильно адсорбционно-активной среды ( расплавленного галлия) позволило доказать, что образующаяся структура является неравновесной. Показано, что протекание процесса обусловлено не ростом энтропии системы, а образованием твердого раствора и снижением упругой энергии, связанной с дислокационной структурой твердого тела. [29]
Исследованию кинетики процесса обычно предшествует изучение ( хотя бы в общих чертах) химии этого процесса. Обычно целесообразно начать изучение какого-либо процесса с экспериментов, дающих качественное представление о его механизме. [30]
Страницы: 1 2 3 4