Исследование - термическое разложение
Cтраница 1
 |
Установка Грассн и Мел-вилла для изучения термического распада манометрическим методом.| Обогреваемая ячейка в уста новке Грасси и Мелвилла. [1] |
Исследование термического разложения в вакууме стабилизированных и нестабилизированных полимеров позволяет получить ответ на ряд вопросов, относящихся к механизму VL кинетике протекающих реакций. [2]
Исследование термического разложения, метана и этана методом одноимпульсной ударной трубы. [3]
Исследование термического разложения некоторых полиолефинов методом пиролитической газовой хроматографии. [4]
Исследование термического разложения Мо ( СО) 8 проведено при 200, причем установлено, что скорости реакций разложения этого комплекса подчиняются уравнению первого порядка. По такому же механизму ( как при УФ-облучении) может идти реакция Мо ( СО) 8 с фос-финами. [5]
Исследование термического разложения топлива в глубоком вакууме представляет определенный научный интерес. [6]
Исследование термического разложения нефтяных смол и асфальтенов: Автореф. [7]
Исследование термического разложения низкомолекулярного полипропилена в вакууме126 позволило установить, пользуясь методом масс-спектрометрии, присутствие в числе летучих продуктов этилена, пропилена, бутана, бутиленов, пентана и др. Изучение механизма термической деструкции высокомолекулярного полимера192, проводившееся в вакууме, показало, что при температуре ниже 300 С деструкция протекает очень медленно. При 412 С в течение 30 мин полипропилен разрушается практически полностью. При этом был установлен цепной механизм реакции распада. Введение такого ингибитора, как дифе-нилолпропан, заметно уменьшает начальную скорость разложения W0, практически постоянную при небольшой глубине превращения. Необходимость добавления довольно больших количеств указанного стабилизатора, по-видимому, связана с испарением или разложением данного препарата, практически мало устойчивого при температуре выше 250 С. [8]
Исследование термического разложения нефтяных смол и асфальтенов / / Автореф. [9]
Исследование термического разложения пылевидного сланца проводилось на лабораторной установке проточного типа, схема которой изображена ниже. [10]
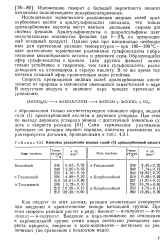 |
Кинетика разложения медных солей ( I арилкарбоновой кислой. [11] |
Исследования термического разложения медных солей арил карбоновых кислот и арилсульфокислот показали, что тольк ( арилкарбоновые кислоты могут явиться реальным сырьем дл5 синтеза фенолов. Однако уже при минимально необходи мых для протекания реакции температурах - при 180 - 190 С - идет интенсивное термическое разложение сульфокислоты с обра зованием коксообразного остатка и двуокиси серы. Образующий эфир сульфокислоты и крезола ( или другого фенола) значи тельно устойчивее к гидролизу, чем сама сульфокислота, распа дающаяся на углеводород и серную кислоту. В то же время тер мически сложный эфир сравнительно мало устойчив. [12]
 |
Диаграмма для определения значения v при термическом разложении н-гек-садекана в проточной системе при атмосферном давлении. [13] |
Исследованиям термического разложения низших парафинов, в частности метана и этана, посвящены многочисленные работы. Это объясняется стремлением выяснить механизм процессов, что важно для промышленного получения этилена или ацетилена пиролизом этана и метана. В превосходной монографии [1] детально рассмотрено состояние работ в этой области примерно до 1953 г. В другой работе [15] описан пиролиз легких углеводородов для получения ацетилена; особое внимание уделяется пиролизу метана. Для более легкой интерпретации кинетических данных много работ было сделано при давлениях ниже атмосферного. Следует подчеркнуть, что предложенные схемы кинетики этих реакций и приводимые ниже замечания относятся главным образом к процессам, проводимым именно при этом условии. [14]
Исследованию термического разложения сульфатов железа посвящено большое количество работ [1-19], в которых рассматриваются закономерности диссоциации ферросульфатов в инертной, восстановительной и окислительной средах. Показано, что добавки восстановителей интенсифицируют процесс термического разложения сульфата двухвалентного железа, так как связывание ими кислорода, выделяющегося при диссоциации SO3, исключает реакцию окисления сульфата двухвалентного железа до трехвалентного. [15]
Страницы: 1 2 3 4