Исследование - термическое разложение
Cтраница 2
Исследованию термического разложения насыщенных перекисных эфиров типа RCO-ОО-R посвящено значительное число работ. Было показано 1 - 3, что в растворах эти эфиры распадаются по свободнорадикальному механизму приблизительно по уравнению первого порядка. В насыщенных перэфирах, в отличие от диалкил - и диацилперекисей, перекисная связь подвержена влиянию различных по электроотрицательности заместителей и некоторые из этих соединений 4 - 6 склонны к гетеролитическому распаду. [16]
Исследованию термического разложения насыщенных перекисных эфиров типа RCO-ОО-R посвящено значительное число работ. Было показано 1 - 3, что в растворах эти эфиры распадаются по свободнорадикальному механизму приблизительно по уравнению первого порядка. В насыщенных перэфирах, в отличие дт диалкил - и диацилперекисей, перекисная связь подвержена влиянию различных по электроотрицательности заместителей и некоторые из этих соединений 4 - 6 склонны к гетеролитическому распаду. [17]
Проведено исследование термического разложения под давлением водяных паров сланца Прибалтийского месторождения при различной температуре, продолжительности нагрева и в присутствии различного количества воды. Показано, что минеральная часть сланца оказывает крекирующее влияние. [18]
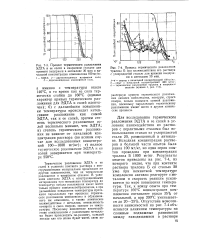
Для исследования термического разложения ЭДТА и ее солей в условиях взаимодействия их растворов с перлитными сталями был использования стакан из углеродистой стали 20, размещенный в автоклаве. Исходная концентрация растворов в большей части опытов была равна 100 мг / кг, но одна серия опытов проведена при концентрации трилона Б 1000 мг / кг. Результаты опытов приведены на рис. 7 - 4, из которого видно, что при контакте раствора трилона Б со сталью 20 уже при комнатной температуре комплексен активно реагирует с металлом и скорость реакции усиливается по мере повышения температуры. [20]
При исследовании термического разложения М М - тиобисами-нов Сейвил и др. 18 нашли, что легче всего в них подвергается разрыву связь S-N с образованием свободного амина и элементарной серы. Можно предположить поэтому, что вулканизация М М - тиобисаминами, например диморфолинилдисульфидом, протекает таким же путем, как и катализированное аминами сульфи-дирование олефинов. Сейвил показал, что эта реакция должна включать полярное присоединение серы к олефиновой двойной связи с последующим образованием диалкилмоносульфидной поперечной связи. [21]
При исследовании термического разложения алифатических нитросоединений и нитроаминов получены характеристики трех мономолекулярных процессов: диссоциации связи С - NO2, элиминирования HNOZ из нитросоединений и разрыва связи N - N02 в нитроаминах. Изучение реакции разрыва связи С - N02 позволяет кинетическим методом определить энергию диссоциации D ( С-IV), которая лежит в пределах 35 - 55 ккал моль, и термохимически оценить теплоты образования нитро-алкильных радикалов. Величина предэкспоненциального множителя k0 меняется от 10 Б до 10 сек-1. Здесь проявляются все факторы, которые, согласно теории, могут влиять на величину k0: понижение частот маятниковых колебаний, освобождение заторможенного внутреннего вращения вокруг связи С - NO2, понижение частот крутильных колебаний соседних с реакционным центром алкильных групп в активированном комплексе. [22]
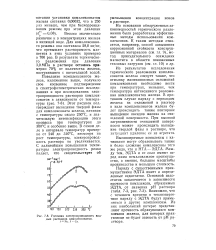 |
Удельная электропроводность водных растворов комплексонатов. [23] |
Из результатов исследования термического разложения комплексонатов железа следует также, что отмывку железоокисных отложений комплексонами необходимо вести при температурах, меньших, чем температура интенсивного разложения комплексонатов железа. [24]
При проведении нами исследования термического разложения первичной гидроперекиси н-амила в растворе хлорбензола в атмосфере азота было установлено образование валериановой кислоты и водорода. В присутствии кислорода глубина и направление процесса меняются. Интересно, что среди разнообразных, развивающихся одновременно направлений термического разложения вторичной гидроперекиси н-амила в изученных условиях идет также реакция с образованием масляной кислоты и метана, но в значительно меньшей степени. [25]
То же было отмечено при исследовании термического разложения тсрфа, когда при его нагревании до 500 за 0 25 сек. [26]
Из опытов Шапатнной и Калюжного [324] по исследованию термического разложения угольной ныли следует, что процесс выделения летучих из мелких частиц сильно отстает во времени от их нагрева, и чем выше скорость нагрева, тем больше отстает процесс термического разложения топлива. [27]
 |
Зависимость температуры начала диссоциации ферроцианидов самария от ионного потенциала металла третьей координационной сферы. [28] |
Как уже отмечалось выше, данные по исследованию термического разложения смешанных ферроцианидов весьма немногочисленны. Имеется указание, что температуры термической диссоциации ферроцианидов железа Fe111 Fe111 [ Fe ( GN) 6 ] 3 и Cs Feni [ Fe ( CN) 6 ] также близки между собой [1275], что свидетельствует в пользу высказанных выше соображений. Однако для окончательного их подтверждения необходимо дальнейшее накопление экспериментального материала. [29]
Вопрос о выборе газа, в котором должно производиться исследование термического разложения ферроцианида, требует особого обсуждения. Известно, что процесс диссоциации не начинается ниже температуры равновесия, если нагревание производится в атмосфере того газа, который выделяется при распаде. С этой точки зрения термическое разложение ферроцианидов должно было бы исследоваться либо в атмосфере циана, либо - в азоте. Поскольку выделение первого обычно происходит ниже 500 С, а второго - при более высоких температурах, применение каждого из названных газов в качестве атмосферы для проведения реакции удобно лишь в определенном температурном интервале. Практически же изучение термического разложения железистосинеродистых солей удобнее проводить в аргоне, который инертен по отношению ко всем продуктам реакции. Если газообмен исключен, то распад уже первых порций вещества увеличивает парциальное давление выделяющегося при разложении газа настолько, что дальнейшее разложение прекращается. Окончательный же распад происходит после достижения температуры равновесия в смеси аргона и того газа, который получается в данном температурном интервале. [30]
Страницы: 1 2 3 4