Потенциометрическое исследование
Cтраница 1
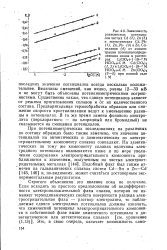
Потенциометрические исследования показали, что в пределах рН б - 10 его восстановление происходит в одну стадию с участием двух электронов на молекулу, но ниже рН б оно протекает в две стадии. На это указывают изменение цвета от красного через зеленый к бесцветному, а также вид кривой, получаемой, если отложить на графике потенциал в зависимости от процента восстановления. Кривые, получаемые при восстановлении в очень кислых растворах, соответствуют термодинамическим уравнениям для образования семихинонов. Как видно из рисунка, зеленый цвет является свойством семихинонов. Следует обратить внимание, что по мере увеличения рН потенциалы первой и второй стадий сближаются друг с другом, пока, наконец, при рН 5 они не становятся идентичными. Выше этой величины рН любой восстановитель, достаточно сильный для образования семихинонов, уже более чем достаточно силен для завершения реакции. Таким образом, с термодинамической точки зрения выше рН 5 одноэлектронные переходы невозможны. [1]
Потенциометрическое исследование подтвердило полярографические данные и позволило доказать, что образование водородных комплексов происходит при наличии бетаиновых водородов в комплексоне. На рис. 3 представлены некоторые из полученных данных. [2]
Потенциометрическое исследование комплексов бериллий - НТА проводилось при концентрации НТА 1.10 - 3 моль. [3]
Потенциометрическое исследование катализатора в процессе восстановления производных нитробензола показало, что присутствие заместителя в молекуле прежде всего отражается на ее адсорбционной способности. [4]
Потенциометрическое исследование системы ион уранила-аскорбиновая кислота. [5]
Потенциометрическое исследование жидкой системы может доставить ряд весьма важных сведений о механизме диссоциативных процессов и переноса тока. Однако в большинстве случаев исследователю приходится сталкиваться с проблемой выбора обратимого индикаторного электрода. [6]
Потенциометрическое исследование комплексов серебра с N, N - бис ( 2-оксиэтил) - дитиооксамидом. [7]
Потенциометрическое исследование хлоридньгх комплексов висмута / / Журн. [8]
Потенциометрическое исследование взаимодействия щелочноземельных элементов с этим комп-лексоном показало, что образуемые комплексы очень слабые и константы устойчивости их не превышают 1 - 2 порядков. [9]
Потенциометрическим исследованием [33] ацетатного комплексообразования трехвалентного железа установлены условия возникновения комплексов FeAc2 1, FeAc. Указывается, что на равновесия в растворе оказывают влияние рН и концентрации реагирующих компонентов, в частности концентрация трехвалентного железа. [10]
При потенциометрических исследованиях на различных по составу образцах было также замечено, что значения потенциалов на эвтектических и доэвтектических по электроотрицательному компоненту сплавах совпадают. Подобный факт был также от - мечен на гальванических сплавах систем Cd-Sn и Zn-Cd [145, 146] и, по-видимому, может считаться достоверным экспериментальным результатом. [12]
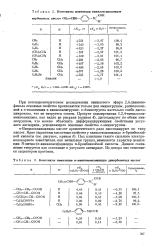 |
Константы ионизации го-ввнилоксиапилидов дикарбоновых кислот. [13] |
При потенциометрическом исследовании винилового эфира 2 4-диамино-фенола основные свойства проявляются только для аминогруппы, расположенной в п-положении к винилоксигруппе. Аминогруппа настолько слабо диссо - - циирована, что не титруется совсем. Продукт ацилирования 1 2 4-винилокси-аминоанилина, как видно из рисунка ( кривая 4), диссоциирует по обеим аминогруппам, что можно объяснить дифференцирующими свойствами уксусного ангидрида, усиливающего основные свойства 0-аминогруппы. [14]
При потенциометрических исследованиях процессов комплек-сообразования используют электроды, обратимые либо по отношению к ионам металла, либо по отношению к лиганду ( анионам) или частицам, находящимся в равновесии с ним. В первом случае определяют концентрацию ( активность) в растворе свободных, не связанных в комплексы ионов металла, а во втором - концентрацию ( активность) свободного, не связанного в комплексы лиганда. Если лиганд обладает кислотно-основными свойствами ( молекулы аммиака, анионы слабых органических кислот и др.), то концентрация свободного лиганда может быть определена путем измерения рН раствора, например, с помощью стеклянного электрода. [15]
Страницы: 1 2 3 4