Потенциометрическое исследование
Cтраница 4
Хотя щавелевокислые комплексы ниобия и тантала были открыты около шестидесяти лет тому назад [1] и их значение в промышленной переработке руд этих металлов, а также при их аналитическом разделении известно, исследованию этих комплексов уделяется чрезвычайно мало внимания. Лишь спустя тридцать лет после открытия оксалатных комплексов ниобия и тантала появляется работа [2], в которой авторы на основании проведенных кондуктометрических и потенциометрических исследований подтверждают факт образования комплексных соединений ниобия и тантала со щавелевой кислотой. В то же время они высказывают предположение, что растворение пятиокисей ниобия и тантала в щавелевой кислоте имеет коллоидный характер. Этими работами в основном и исчерпывается литература, посвященная изучению оксалатных растворов ниобия и тантала. [46]
Так, в зоне разгрузки Узон-Гейзерной гидротермальной мине-ралообразующей системы Камчатки, в пределах термальных полей кальдеры вулкана Узон, имеются участки, на которых формирование рудных сульфидных залежей происходит как на подвижном, так и на неподвижном геохимических барьерах. Закономерности изменения концентраций рудных элементов, типичные для геохимического барьера третьего рода ( см. рис. 11 0), были выявлены в ходе аналитических и потенциометрических исследований, проведенных Г. А. Карповым и А. Л. Павловым на термальных полях Узона. [47]
Михаэлис и Хилл нашли, что продукты окисления дифенил-я-фенилендиамина вполне устойчивы. Симметричный дифенил-я-фенилендиамин ( азофенилен) был описан Бандровским 4, как красный краситель. На основании потенциометрических исследований Михаэлис и Хилл пришли к выводу, что окисление этого индикатора происходит в две ступени и что промежуточный продукт является се-михиноном. [48]
И наконец, в третьем завершающем этапе обычно имеют дело с общеизвестными методами расчета констант, применяемыми независимо от измеряемого физико-химического параметра. Известны различные численные и графические методы, основанные на использовании ряда вспомогательных функций, а следовательно, тех или иных приемов вычислений. Поэтому в дальнейшем без подробного рассмотрения общих принципов расчетных методов будут показаны примеры наиболее типичных потенциометрических исследований химического равновесия. [49]
К электродам первого рода относятся такие, у которых электродная реакция происходит только между металлом электрода и его катионами, находящимися в растворе. В эту группу входят водородный, ртутные, серебряные, медные, свинцовые, платиновые, золотые и другие электроды, применяемые для потенциометрических исследований. Однако большинство металлов, которые могли бы быть использованы для регистрации равновесных потенциалов в качестве электродов первого рода, не нашли применения, так как чистые металлы быстро окисляются, их поверхность покрывается пленкой химических соединений, в результате чего искажается электродная функция. Электродами второго рода называются металлические электроды, находящиеся в контакте с раствором, насыщенным малорастворимой солью металла и содержащим избыток другой соли с одинаковым анионом, концентрация которых в контролируемом растворе и определяет электродный потенциал. Поэтому электроды этой группы используются в основном для измерения активности ионов. Представителями этой группы являются хлорсеребряный, сульфатный и каломельный электроды. [50]
Спектрофотометрию в ультрафиолетовой и видимой областях не следует рассматривать как самостоятельный метод исследования комплексообразования. Обычно спектрофотометрический метод дополняет потенциометрический. Более того, известны случаи, когда невозможно различить равновесные процессы на основании только потенцио-метрических результатов. При проведении потенциометрических исследований необходимо располагать соответствующими электродами, поэтому потенциометрический метод применим для изучения немногих реакций. Недавно вышел обзор [1], в котором обсуждается применение спектрофотометрии для определения констант устойчивости. Некоторые ограничения спектрофотомет-рического метода уже обсуждались в разд. [51]
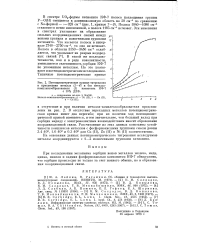 |
Потенциометрические кривые титрования. [52] |
Полоса 1040 - 1080 см-1 становится менее интенсивной, а полоса 1185 см 1 исчезает. Эти изменения в спектрах указывают на образование сильных координационных связей между ионами уранила и ионогенными группами катионита. Что касается полосы в интервале 2740 - 2750 см-1, то она не исчезает. В такой же последовательности, как и в ряде ковалентности, уменьшается селективность сорбции КФ-7 по указанным металлам. На это указывают и потенциометрические исследования. [53]
Страницы: 1 2 3 4