Потенциометрическое исследование
Cтраница 2
Производилось также потенциометрическое исследование катализатора, по методу одного из нас [ в ], позволяющее следить за количеством водорода на поверхности катализатора в ходе реакции. [16]
 |
Электролитическая ячейка для потенциометрического титрования. [17] |
Установка для потенциометрических исследований состоит из ячейки с исследуемым раствором, мешалки, индикаторного электрода, электрода сравнения, бюретки с титрующим раствором и системы регистрации ЭДС. [18]
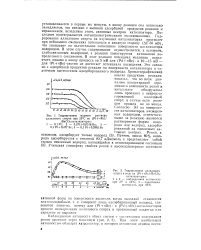 |
Гидрирование водного раствора аллилового спирта при 25 С на ( Pt nRe.| Гидрирование аллилового спирта в воде на ( Pt rcRc / BaCO3. [19] |
Последнее подтверждается потенциометрическими исследованиями. В этом случае гидрирование осуществляется, в основном, слабосвязанным водородом, а реакция лимитируется активацией непредельного соединения. В ходе реакции потенциал медленно возрастает, однако к концу процесса на 5 мВ для ( Pd nRe) - и 10 - 15 мВ - для ( Pt Re) - систем не достигает потенциала насыщения. Это связано с адсорбцией продуктов реакции на поверхности катализатора и частичным вытеснением адсорбированного водорода. [20]
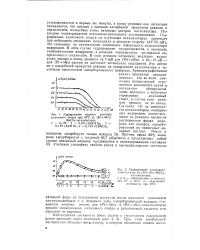 |
Гидрирование водного раствора аллилового спирта при 25 С на ( Pt nRe.| Гидрирование аллилового спирта в воде на ( Pt nRe / BaCOa. [21] |
По-следнее подтверждается потенциометрическими исследованиями. В этом случае гидрирование осуществляется, в основном, слабосвязанным водородом, а реакция лимитируется активацией не предельного соединения. В ходе реакции потенциал медленно возрастает, однако к концу процесса на 5 мВ для ( Pd nRe) - и 10 - 15 мВ - для ( Pt - f - rtRe) - систем не достигает потенциала насыщения. Это связано с адсорбцией продуктов реакции на поверхности катализатора и частичным вытеснением адсорбированного водорода. [22]
Поэтому при потенциометрических исследованиях комплексов металлов, в особенности при их низких концентрациях, необходимо использовать тщательно очищенные реактивы и растворители, удалять из изучаемой системы молекулярный кислород и другие примеси, которые могуг участвовать в необратимых реакциях. Далее рассматриваются гальванические элементы с переносом, содержащие большой избыток постороннего электролита. Предполагается, что диффузионным потенциалом можно пренебречь. [23]
Различают две группы потенциометрических исследований: прямой потенциометрический анализ и потенциометрическое титрование. Первый применяют тогда, когда на индикаторном электроде в исследуемом растворе могут протекать лишь процессы, строго обратимые относительно определяемых ионов раствора и никакие побочные реакции невозможны. Таковы, например, стеклянный водородный электроды и некоторые металлические электроды, покрытые оксидной пленкой. [24]
Существуют две возможности потенциометрического исследования комплексообразования: 1) определить концентрацию-свободных ионов металла, а следовательно, и концентрацию ионов металла, участвующих в комплексообразовании; 2) измерить концентрацию свободных лигандов. Во многих случаях полезно, если это экспериментально возможно, определить обе концентрации. [25]
Поэтому обычная методика потенциометрического исследования комплексообразования в условиях постоянной ионной силы или большого и постоянного фона инертного электролита ( NaC104) неприменима в случае феррицениевых катионов или, по крайней мере, необходима ее заметная модификация. Последняя заключается в выборе более инертного, нежели перхлорат натрия, солевого фона. [26]
Разработана установка для потенциометрического исследования кинетики реакций, включающих вещества, образующие окислительно-восстановительные системы. Проведено потеыциометрическое исследование кинетики взаимодействия брома с формиат-ионами в интервале температур 19 - 50 С. На основании экспериментально определенных порядков реакции по [ Н ], [ HCOif ], [ Br - ] предложен механизм реакции, включающий в качестве промежуточного продукта комплекс ( С а) 8 - Определена энергия активации реакции, равная 18 3 ккал / моль. [27]
Дальнейшие опыты по потенциометрическому исследованию системы La ( NO3) j - K4 [ Fe ( CN) e ] - H2O будут приведены ниже. [28]
Рассматривая суммарную картину, полученную из кондукто-метрических и потенциометрических исследований и препаративных экспериментов, можно отметить: в растворе существует несколько типов ионов, что приводит к образованию сольватов указанных выше составов. Связь фосфорилхлорида с алюминием в этих сольва-тах вероятнее всего осуществляется через кислородный мостик. По-видимому, ион AlCli является единственным анионом в растворе. Существование ионов AlClf и А1С1 - не доказано. [29]
Тех условий, которые существовали при потенциометрических исследованиях, проводившихся с целью показать образование центров основного обмена, не имеется при получении большинства промышленных катализаторов крекинга, хотя описанные выше явления, несомненно, и здесь играют важную роль. Как уже указывалось, в производстве многих шариковых и микросферических катализаторов гидролиз соли алюминия обычно проводят в присутствии геля SiOa, уже полимеризованного при старении. Если гель окиси кремния подвергался старению значительное время, кривая титрования поднимается вверх и достигает точки, которая соответствует соосаждению гидроокиси алюминия. В этом случае, для нейтрализации требуется только три эквивалента щелочи на 1 моль алюминия. [30]
Страницы: 1 2 3 4