Кинетическое исследование
Cтраница 3
Кинетические исследования показали [187], что эти реакции в водных растворах являются реакциями второго порядка и их константы скорости k ( л / люль-сек) при 25 имеют следующие значения: 1 1 - К) 1, 2 2 - 10 и 7 0 - 10е, если Y - С1 -, Вг - и Г соответственно. [31]
Кинетические исследования 149, 52 ] показывают, что в обоих случаях скорость обмена не зависит от концентрации СО, но зависит от концентрации карбонила металла в первой степени. [32]
Кинетические исследования могут принести пользу и в других областях. С другой стороны, правильное применение термодинамических законов, например в металлургии, нередко в значительной мере способствует оптимизации промышленных процессов. [33]
Кинетические исследования [113] показали, что во всех подобных реакциях в определяющей скорость стадии участвуют алкилгалогенид и ион серебра. Стадия реакции, определяющая ее скорость, протекает в основном на поверхности любой присутствующей нерастворимой серебряной соли, в том числе и на образующемся и осаждающемся галогениде серебра, и на первоначально внесенном нерастворимом продукте, например на окиси серебра. Эти реакции, описываемые как 8к1 - подобное замещение, инициируются ионизацией галогенсодержащего соединения на поверхности серебряной соли при помощи адсорбированных ионов серебра. [34]
Кинетические исследования показывают, что как диенофил этот реагент несколько более реакционноспособен, чем тетрацианэтилен. [35]
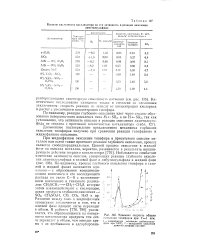 |
Удельная скорость общего окисления тиоэфиров при Г1 атм. [36] |
Кинетические исследования находятся также в согласии со сделанным заключением: скорость реакции не зависит от концентрации кислорода и растет с увеличением концентрации тиоэфира. [37]
Кинетические исследования в этой области, по-видимому, не проводятся. [38]
Кинетические исследования значительно способствовали выяснению механизма реакций полимеризации. Кажущаяся сложность этих реакций устраняется, если принять гипотезу ( впрочем, крайне вероятную), что скорость реакции полимерного радикала с молекулами мономера одна и та же независимо от его длины; активный центр на конце растущего макрорадикала находится исключительно под влиянием атомов радикальной цепи, расположенных непосредственно по соседству с ним, причем эти атомы всегда тождественны при любой длине макрорадикала. [39]
Кинетические исследования [3] показали, что в присутствии простых эфиров реакция протекает с большой скоростью при комнатной температуре; следы эфира действуют на эту реакцию каталитически. [40]
Кинетические исследования, проведенные Доусоном [29] и недавно переосмысленные Свэном [30], подтверждают скорее именно эту точку зрения, а не противоположное мнение, что для енолизации достаточно только одного реагента: кислоты или основания. [41]
Кинетические исследования в данном случае осложнены тем, что в этом мономере удерживаются примеси, которые существенно влияют на полимеризацию. С повышением чистоты сильно повышается чувствительность N-винилпирролидона к кислороду; при соприкосновении с гидратом окиси натрия или калия образуются вещества, действующие как замедлители. [42]
Кинетические исследования показывают, что достаточно реакционноспособные ароматические соединения нитруются со скоростью, не зависящей от их концентрации. Следовательно, существует медленная стадия реакции, в которой нитруемое соединение не принимает участия. По общему правилу химической кинетики именно эта медленная стадия и определяет суммарную скорость. [43]
Кинетические исследования обычно проводят при низкой конверсии мономеров, чтобы избежать необходимости учета реакций разветвления полимеров. Принимается принцип квазистационарного состояния, при котором скорость образования начальных активных центров полимеризации равна скорости обрыва цепи путем рекомбинации. [44]
Кинетические исследования показывают, что щелочное плавление - не всегда реакция третьего порядка. [45]
Страницы: 1 2 3 4