Длина - водородная связь
Cтраница 4
Это обстоятельство позволяет использовать кривую 2 ( рис. 8.1) в качестве универсального потенциала О - - Н в пептидах. Имеющиеся экспериментальные данные по длинам водородных связей в амидах [40] находятся в области минимума этой кривой. [46]
Исследования Бржана [19] были посвящены изучению состояния воды, адсорбированной на силикагеле. Кроме характеристик нескольких аммонийных комплексов автор приводит длины водородной связи в гидратах NH3 - H. [47]
Однако энергия водородной связи вначале очень слабо убывает по мере увеличения угла изгиба. По этой же причине для удовлетворения стерических требований длина водородной связи может слегка изменяться без ее разрыва. [48]
Изменение электронной плотности на ОН-связи, которое происходит при образовании водородного мостика, меняет не только ее силовую постоянную, но также и ЭОП. Поэтому абсолютные интенсивности всех переходов, при которых меняется длина водородной связи или прилежащий к ней угол, тоже должны нести в себе информацию об энергии Н - связи. [49]
Реакции этих катионов более определенны, более однозначны по сравнению с реакциями катионов других металлов, для которых координационные числа, как правило, выше и могут изменяться в зависимости от условий. Кроме того, стереохимические требования небольшого атома в хелатах соответствуют длинам мостиковых водородных связей, изменяющимся от 2 4 до 2 6 А [1902, 2253, 2254] в хелатах протона. [50]
Аккерман [37] рассматривали комплекс воды Они считают, что протон с иона Н3О перескакивает на молекулу воды во вторичной гидратной оболочке. Согласно этой теории, движущийся в некоторой мере свободно протон совершает несколько колебаний между первичным ионом НзО и вторичной гидратной оболочкой, прежде чем центр комплекса как целого сместится на расстояние, равное длине водородной связи. [51]
Вг - - приводят к образованию сравнительно длинных водородных связей. Если бы их длины были исправлены на разность между вандерваальсовыми радиусами С1 и Вг ( 1 75 и 1 85 А соответственно) и теми же параметрами для О и N ( 1 52 и 1 55 А), то они оказались бы значительно более длинными и, следовательно, менее прочными, чем водородные связи с другими акцепторными группами, перечисленными в табл. 4.2. Например, если донором является группа ( W) O - Н, то исправленные длины водородных связей с С1 - и Вг - имеют значения соответственно 2 92 и 3 07 А. [52]
Мочевина является исключением среди амидов в том отношении, что в ней имеются четыре группы N - Н на одну молекулу в дополнение к одному атому кислорода. О для водородных связей, в которых мочевина одновременно играет роль донора и акцептора, характеризуется средним значением 2 98 А и пределами от 2 81 до 3 13 А. Длина водородных связей, в которых карбонильная группа мочевины играет роль акцептора, всегда меньше - от 2 70 до 2 80 А. [53]
 |
Компоненты смещений о, г по осям а, Ь. [54] |
Большой вклад в понимание энергетической устойчивости экспериментально наблюдаемых политипов из двухэтажных слоев дала работа [10] по определению структуры дмжита. Найденные особенности строения отдельных слоев: угол дитригонального разворота тетраэдров 7 5 и неплоская поверхность атомов О оснований тетраэдров ( один из трех атомов О опущен в глубь двухэтажного слоя на 0 17 А по сравнению с остальными) - обусловливают неравноценность тетраэдри-ческих атомов О в отношении их участия в образовании водородных связей. Действительно, если длина водородной связи с гидроксильными поверхностями Октаэдров для двух атомов О тетраэдров составляет 2 94 и 2 97 А, то для третьего - опущенного - она равна 3 12 А, что отвечает очень слабой водородной связи. [55]
Это ограничивает возможность образования пар оснований. Два пурина не могут совместиться в пространстве, а два пиримидина будут расположены слишком далеко друг от друга, чтобы между ними могла образоваться водородная связь. Образование пар оснований определяется длиной водородной связи: аде-нин соединяется с тимином, а гуанин - с цитозином или 5-метил-цитозином ( фиг. Такое расположение объясняет соответствие, найденное для относительного содержания оснований ДНК. [56]
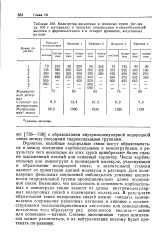 |
Количества кислотных и основных групп ( мг-экв на 100 г материала в продукте конденсации п-аминобензойной кислоты с формальдегидом и в четырех фракциях, выделенных из него. [57] |
Вероятно, подобные водородные связи могут образовываться и между соседними карбоксильными и аминогруппами, в результате чего некоторые из этих групп приобретают более сильно выраженный кислый или основный характер. Число карбоксильных или аминогрупп в полимерной молекуле, участвующих в образовании водородной связи, в значительной степени зависит от ориентации данной молекулы в растворе. Для полиядерных фенольных соединений наблюдалось усиление кислотности гидроксильной группы пропорционально длине водородной связи. Возможно, что кислотность и основность карбоксильных и аминогрупп также зависит от длины внутримолекулярных водородных связей в полимерных молекулах. В результате образования таких водородных связей можно ожидать возникновения сопряжения различных катионов и анионов с соответствующими недиссоциированными кислотами или основаниями, вследствие чего образуется ряд комплексов кислота - анион или основание - катион. Степень диссоциации таких комплексов может различаться, и их нейтрализация поэтому будет протекать по-разному. [58]
Страницы: 1 2 3 4