Длина - ковалентная связь
Cтраница 1
Длины ковалентных связей обычно определяют рентгеноструктурным анализом. Половина длины ковалептной связи в симметричной молекулет например C1 - G1, называется ковалентным радиусом элемента. После того-как ковалентный радиус атома измерен, можно определить длину связи между этим и другим атомом и по разнице определить ковалентный радиус второго атома. [1]
Длина ковалентных связей составляет 0 1 - 0 19 нм, а энергия - 210 - 480 кДж / моль. [2]
 |
Схематическое изображение сечения кристалла.| Схематическое изображение кристаллической решетки вещества, состоящего из полярных молекул. [3] |
Длина ковалентной связи I - I равна 2 82 А, а длина ион-дипольной связи в образовавшемся молекулярном ионе достигает 3 10 А. [4]
Длины ковалентных связей одинаковой кратности между одноименными атомами являются примерно постоянными. [5]
Половина длины ковалентной связи в симметричной молекуле, например С1 - С1, называется ковалентным радиусом атома элемента. [6]
Строго говоря, длина ковалентной связи не имеет одного определенного значения, так как два связанных ею атома постоянно находятся в движении друг относительно друга. [7]
Межъядерное расстояние ( длина ковалентной связи) - величина аддитивная, она равна примерно сумме ковалентных радиусов двух связанных между собой атомов. [8]
Поскольку для молекулы СоН длина ковалентной связи составляет 1 593 А [10], расчетные данные, согласно которым длина связи Со - Н составляет 1 2 А, подтверждали правильность взгляда Гибера. [9]
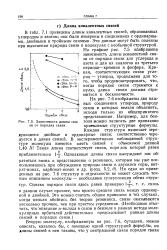 |
Зависимость длины свя - зи от порядка связи. [10] |
В табл. 7.1 приведены длины ковалентных связей, образованных углеродом и азотом; они были измерены в соединениях с ординарными, двойными и тройными связями. Эти данные могут быть полезны при выяснении природы связи в молекулах с необычной структурой. [11]
На графике рис. 7.5 изображена зависимость длины ковалентной связи от порядка связи для углерода и азота и для их аналогов из третьего периода-кремния и фосфора. Кривая, соответствующая связи углерод - углерод, продолжена для того, чтобы продемонстрировать, что, когда порядок связи стремится к нулю, длина связи должна стремиться к бесконечности. [12]
Структурные исследования привели к заключению, что длины ковалентных связей в хорошем приближении можно рассматривать как инварианты, а это позволяет заключить, что не меняются и атомные радиусы. [13]
 |
Ковалентные и вандерваальсовы радиусы для водорода и хлора. [14] |
Сумма ковалентных радиусов хлора и водорода равна длине ковалентной связи в хлориде водорода ( рис. 4.7); на этом же рисунке приведены также вандерваальсовы радиусы, подробнее о которых будет сказано в разд. [15]
Страницы: 1 2 3 4