Длина - двойная связь
Cтраница 2
Против наличия в таких молекулах семиполярных связей свидетельствует то, что длина связей приближается к длине обычных двойных связей, в то время как длина семиполярных связей близка к длине простых связей; дипольные моменты рассматриваемых соединений значительно меньше дипольных моментов, рассчитанных при допущении семиполяр ых связей; связи серы, фосфора и хлора с кислородом в рассматриваемых соединениях прочнее, чем типичные семиполярные связи. [16]
Против наличия в таких молекулах семиполярных связей свидетельствует то, что длина этих связей приближается к длине обычных двойных связей, в то время как длина семиполярных связей близка к длине простых связей; дипольные моменты рассматриваемых соединений значительно меньше дипольных моментов, рассчитанных при допущении семиполярных связей; связи серы, фосфора и хлора с кислородом в рассматриваемых соединениях химически прочнее, чем типичные семиполярные связи. [17]
Основным свойством ароматических соединений можно назвать то, что длины связей в циклах составляют среднее между значениями длин одинарных и двойных связей. [18]
Так, длина одинарной связи S - N в молекуле HSO3 ( NH2) равна 174 пм, а длина двойной связи S - N в S4N2F4 - - 154 пм. [19]
В ароматических соединениях, где три двойных связи распределены на шесть атомов, ее длина занимает промежуточное положение между длинами одинарных и двойных связей. [20]
Строение сильно полярной / / 1 6 D) молекулы S02 - угловое, ( sp - гибридизация АО серы), угол 119 5, длина двойной связи S - О равна 143 пм. [21]
В настоящее время известно, что молекула бензола образует плоский правильный шестиугольник со следующими параметрами: внутренние углы равны 120, расстояние между атомами углерода-1 39 А, промежуточное между длиной простой связи-1 54 А и длиной двойной связи - 1 33 А. Молекула не напряжена, так как три валентности вокруг трпгоналыюго атома углерода - С-расположены в одной плоскости и направлены под углом 120J один относительно другого. Повышение устойчивости ядра обеспечивается за счет взаимодействия или сопряжения двойных связей структуры Кекуле, и этот эффект был количественно определен из теплоты сгорания и теплоты гидрогенизации. Он приблизительно равен 39 ккал / моль, из чего можно сделать заключение, что реакционная способность бензола энергетически гораздо ближе к реакционной способности насыщенного парафина, чем к реакционной способности олефипа. Величина 39 ккал представляет собой резонансную энергию бензола; значение ее становится особенно заметным, если сравнить ее с величиной резонансной энергии, 1 3-бута-дпена, которая равна только 3 - 4 икал. [22]
S-О, которое подчеркивает полярность связи S-О, и ( 2) 0, которое лучше согласуется с такими свойствами этой группы, как длина S-О - связи ( в диметилсульфоксиде длина S-О - связи составляет 147 пм [1], в то время как длины одинарной и двойной Связи сера-кислород составляют соответственно 169 и 149 пм [2]), относительно малый момент S-О - связи в сравнении с N - - О-связью в оксидах аминов и высокие значения силовой постоянной связи S-О. Автор наиболее полного обзора [4] придерживается компромиссной точки зрения и полагает, что порядок связи S - О зависит от природы R и R1 и может коррелировать с данными по валентным колебаниям в ИК-области спектра. [23]
 |
Схематическое изображение электронного строения этилена ( разные формы изображения а - и я-связи. [24] |
О том, что две связи между атомами углерода не являются простым удвоением одинарной связи, свидетельствуют многие физические данные, например, длина связи, ее энергия и др. Как указывалось выше, длина простой связи С - С равна 1 54 А, а длина двойной связи С С - 1 34 А; энергия связи С - С равна 350 кДж / моль, а энергия двойной связи С С - 606 1 кДж / моль. Разница в 256 1 кДж / моль и является приблизительной мерой прочности л-связи. [25]
О или S-О, которое подчеркивает полярность связи S-О, и ( 2) SO, которое лучше согласуется с такими свойствами этой группы, как длина S-О - связи ( в диметнлсульфоксиде длина S-О - связи составляет 147 пм [1], в то время как длины одинарной и двойной связи сера-кислород составляют соответственно 169 и 149 пм [2]), относительно малый момент S-О - связи в сравнении с N-О - связью в оксидах аминов и высокие значения силовой постоянной связи S-О. Автор наиболее полного обзора [4] придерживается компромиссной точки зрения и полагает, что порядок связи S-О зависит от природы R и R1 и может коррелировать с данными по валентным колебаниям в ИК-области спектра. [26]
Однако если считать, что связи между атомами 1, 2 и 3, 4 являются двойными, а центральная связь С2 - С3 простой, то соответствующие межатомные расстояния должны были бы равняться 1 32 и 1 54 А, в то время как на самом деле длина двойной связи в молекуле бутадиена оказывается равной 1 35 А, а простой - 1 46 А. [27]
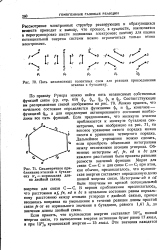 |
Пять независимых валентных схем для реакции присоединения.| Симметричное приближение этилена к бутадиену ( / - нормальная длина двойной связи. [28] |
В первом приближении предполагалось, что расстояния a /, fe, ed и be в начальном состоянии равны нормальному расстоянию между атомами углерода с двойной связью, причем вводилась поправка на уменьшение в течение реакции длины простой связи fe от ее нормального значения в бутадиене, равного 1 41 А, до значения длины двойной связи. [29]
 |
Расположение р-обла-ков в бензоле. [30] |
Страницы: 1 2 3 4