Длина - двойная связь
Cтраница 4
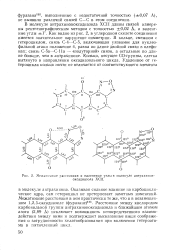 |
Межатомные расстояния и валентные углы в молекуле антрахиноноксадиазола ХСИ. [46] |
Как видно из рис. 2, в углеродном скелете соединения имеется значительное нарушение симметрии. В кольце, смежном с гетероциклом, связь С-4-С-5, включающая уязвимое для нуклео-фильной атаки положение 4, равна по длине двойной связи в олефи-нах; связь С-5 а - С-11 а - полуторной связи, а остальные по длине больше, чем в антрахиноне. Кольцо, несущее СО-группы, слегка вытянуто в направлении оксадиазольного цикла. [47]
 |
Координаты, используемые для анализа реакции СН20 Н . [48] |
Оно определяется целиком классическими ион-ди-лольными взаимодействиями, поскольку перекрывание орбиталей равно нулю. Приблизительно при 2 5 А ковалентные эффекты начинают брать верх; величина угла а приближается к своей конечной величине - углу тетраэдра, расстояние С-О изменяется от длины двойной связи до длины простой связи, а атомы водорода метиленовой группы опускаются ниже плоскости. Энергия монотонно падает, и барьер отсутствует. [49]
Галогениды сульфурила, SO2X2, являются еще одним примером шестивалентных тетраэдрических молекул с двумя я-связями. Например, в сульфурилфториде ( 64 Г) углы OSO и FSF равны соответственно 124 и 96 1, а расстояния S-О ( 143 пм) соответствуют длинам двойных связей. [50]
Рассмотрим, какими эффектами сопровождается увеличение в молекуле длины системы сопряженных связей. Ленард - Джонс70, используя для расчетов метод молекулярных орбиталей, пришел к заключению, что по мере удлинения полиеновой цепи на больших расстояниях от концов молекулы должно происходить полное выравнивание длин ординарных и двойных связей. Однако последующее теоретическое рассмотрение71 показало, что альтернирование длин ординарных и двойных связей сохраняется в полиеновых системах любой протяженности. Недостаточная точность расчетов Ленард-Джонса обусловлена отсутствием учета периодического потенциала, создаваемого скелетом макромолекулы, образованным из атомов углерода, соединенных о-связями. [51]
Метод Хюккеля был использован в работе [174] для установления электронной плотности в молекуле бутадиена-1 3, адсорбированной на поверхности окисного молибденового катализатора, нанесенного на окись титана. Один тип связи молекулы бутадиена с поверхностью характеризуется более положительным зарядом на 1-ом и 4-ом атомах углерода по сравнению с 2-ым и 3 - м, в другом случае все атомы углерода нейтральны, а длина связи между 2-ым и 3-им атомами С примерно равна длине двойной связи. [52]
Полное описание химической связи металла с олефином, разработанное Чаттом, Дьюаром и Дункансоном, включает в себя как а, так и л-взаимодействие. В отличие от карбонильных лигандов, являющихся всегда л-акцейторами, олефиновые лиганды в зависимости от природы металла могут быть преимущественно либо о-донорами, либо 71-акцепторами. Длина координированной двойной связи не отличается существенно от длины связи GC в свободном олефине. [53]
Данные рентгеноструктурного анализа и измерения дифракция электронов ( Робертсон, 1951) подтверждают химические исследования. В то время как для бензола длина любой связи С-С составляет 1 40 А, что является средним между длиной алифатической ординарной связи ( 1 54 А) и двойной связи ( 1 33 А), у нафталина длина связей другая. Несоответствие этих расстояний длинам алифатических ординарных и двойных связей указывает на наличие определенной резонансной стабилизации; химическое поведение означает только фиксацию связей в части молекулы, подвергающейся замещению, и отсутствие резонансной стабилизации в другой части. [54]
Данные рентгеноструктурного анализа и измерения дифракции электронов ( Робертсон, 1951) подтверждают химические исследования. В то время как для бензола длина любой связи С-С составляет 1 40 А, что является средним между длиной алифатической ординарной связи ( 1 54 А) и двойной связи ( 1 33 А), у нафталина длина связей другая. Несоответствие этих расстояний длинам алифатических ординарных и двойных связей указывает на наличие определенной резонансной стабилизации; химическое поведение означает только фиксацию связей в части молекулы, подвергающейся замещению, и отсутствие резонансной стабилизации в другой части. [55]
С), растворимый в эфире. Он в высшей степени реакционноспособен, тотчас реагирует с кислотами, но устойчив к действию щелочей. С - N - промежуточная между длиной ординарной и двойной связи, а длина связи N N - промежуточная между длиной двойной и тройной связи. [56]
Рассмотрим, какими эффектами сопровождается увеличение в молекуле длины системы сопряженных связей. Ленард - Джонс70, используя для расчетов метод молекулярных орбиталей, пришел к заключению, что по мере удлинения полиеновой цепи на больших расстояниях от концов молекулы должно происходить полное выравнивание длин ординарных и двойных связей. Однако последующее теоретическое рассмотрение71 показало, что альтернирование длин ординарных и двойных связей сохраняется в полиеновых системах любой протяженности. Недостаточная точность расчетов Ленард-Джонса обусловлена отсутствием учета периодического потенциала, создаваемого скелетом макромолекулы, образованным из атомов углерода, соединенных о-связями. [57]
Страницы: 1 2 3 4