Карбид - литий
Cтраница 3
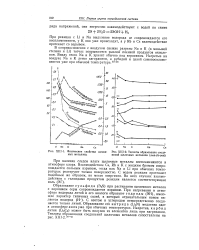 |
Физические свойства щелоч - [ IMAGE ] ХЩ-2. Теплоты образования соеди-ных металлов. нений щелочных металлов ( ккал / г-экв. [31] |
Образование сульфида ( Э25) при растирании щелочного металла с порошком серы сопровождается взрывом. С азотом и углеродом непосредственно соединяется только литий. Образование его нитрида ( Li3N) медленно идет в атмосфере азота уже при обычных температурах. Напротив, карбид лития ( LJ2C2) может быть получен из элементов лишь при нагревании. [32]
Карбид лития LizC2 является сильным восстановителем. При комнатной температуре горит в атмосфере фтора и хлора, при нагревании - в атмосфере брома и иода, при сильном нагревании - в атмосфере кислорода, серы, селена. Карбид лития с фосфором образует фосфид. При температуре 650 - 700 С карбид лития взаимодействует с мышьяком; в расплавленном состоянии он окисляется хлоратом и нитратом калия. [33]
В сухой камере готовят шихту стехиометрическото состава из 20 г гидрида лития и 30 25 г сажи. Сажу обезвоживают предварительным прокаливанием в вакууме при 400 и остаточном давлении 0 2 мм. Реторту с загруженной в нее шихтой устанавливают в электрическую печь и присоединяют к форвакуумному насосу. При достижении в системе вакуума 0 2 мм включают нагрев печи. Учитывая, что карбид лития начинает диссоциировать на металлический литий и углерод с 600, температуру поднимают до 650 постепенно. При 650 ( допустимые отклонения температуры 25) шихту выдерживают в течение шести часов, после чего охлаждают в вакууме до комнатной температуры. При этом литий частично уносится из зоны реакции. [34]
Гидрид лития получается гидрированием расплавленного лития водородом. В отсутствие воздуха плавится при 690 С без разложения. С водой реагирует, как и все солеобразные гидриды, с выделением водорода и образованием гидроксида лития, а кислородом окисляется только при температуре красного каления. Скорость образования нитрида резко возрастает при 250 С. Он плавится без разложения при 845 С, а при растворении в воде выделяет аммиак и LiOH. Карбид лития является сильным восстановителем, а при нагревании термически диссоциирует на литий и графит. В отличие от углерода кремний образует с литием силициды Li4Si и Li2Si, отвечающие правилам формальной валентности. [35]
При наличии следов влаги щелочные металлы воспламеняются в атмосфере хлора. Взаимодействие Cs, Rb и К с жидким бромом сопровождается сильным взрывом, тогда как Na и Li при обычных температурах реагируют только поверхностно. С иодом реакции протекают энергично лишь при подогревании. Образование сульфида ( Э25) при растирании щелочного металла с порошком серы сопровождается взрывом. С азотом и углеродом непосредственно соединяется только литий. Образование его нитрида ( Li3N) медленно идет в атмосфере азота уже при обычных температурах. Напротив, карбид лития ( Li2C2) может быть получен из элементов лишь при нагревании. [36]
Страницы: 1 2 3