Карбоангидраза
Cтраница 3
Были также найдены сфингомиелиназа [ 13 и карбоангидраза. При исследовании субстратной специфичности установлено, что галактозилцереброзид и фос-фатидилсерин активируют активность холестеролэстеразы, а ган-глиозид и лизолецитин, наоборот, ингибируют ее. Четкие физиологические функции ферментов миелиновой оболочки пока еще не обнаружены. [32]
 |
Роль системы плазма-эритроцит в дыхательной функции крови ( по. [33] |
Образующаяся угольная кислота быстро расщепляется при участии карбоангидразы на углекислый газ и воду. Низкое РС02 в просвете альвеол способствует диффузии углекислого газа из эритроцитов в легкие. [34]
Ионы Zn2 1 присутствуют также в молекулах карбоангидразы, катализирующей гидратацию СО2 до Н2СО3 и протеолитического фермента карбокси-пептидазы, секретируемого в тонкий кишечник. Гормон инсулин накапливается в виде комплекса с цинком. [35]
Одна группа таких данных касается изменений количества карбоангидразы, происходящих при изменении содержания ССЬ в окружающей среде. Как правило, при дефиците С02 содержание фермента высокое; при обилии СО2 этот высокий уровень не сохраняется. Например, если клетки Chlorella, росшие в богатой СО2 среде, перенести в среду с низким содержанием СО2, они будут примерно в течение получаса неспособны к фотосинтезу. [36]
 |
Клетки Chlorella, росшие в среде, богатой СО2, и затем перенесенные в среду с низким содержанием СО2, в течение примерно 30 мин неспособны к фотосинтезу. [37] |
Вторая группа данных, свидетельствующих о связи карбоангидразы с фотосинтезом, была получена при обработке растений специфическими ингибиторами этого фермента. В большинстве случаев такие яды резко снижают интенсивность фотосинтеза. [38]
Методами потенциометрического и спектрофотометрического титрования обеих форм карбоангидразы человека [69, 70] и изо-фермента В быка [71] были получены детальные кривые титрования в области ионизации гидроксильной группы тирозина. Эти семь групп, по-видимому, являются скрытыми в глубине молекулы остатками гистидина. Четыре остальных гисти-дина в нативном белке титруются нормально. При обратном титровании щелочью от рН2 число групп, титруемых при рН 5 - 8, возрастает до И. [39]
При 10 - 8 М неконкурентно ин-гибирует карбоангидразу. [40]
В эритроцитах млекопитающих эта реакция, катализируемая карбоангидразой, играет большую роль в удержании метаболической СО2 внутри клетки и таким образом облегчает ее быстрый перенос от активно дышащих тканей к легким. Незаряженная молекула газа ( СО2) относительно быстро диффундирует и может легко проникать в эритроцит. [41]
Величина магнитной восприимчивости Со ( П) - карбоангидразы согласуется с несколькими вариантами тетраэдрической геометрии. К сожалению, интерпретация тонких различий восприимчивости невозможна. Независимо от силы поля лигандов тетраздрические комплексы Со ( II) являются высокоспиновыми вследствие распределения орбитальных энергетических уровней. Со ( Н) - карбоанги-драза остается высокоспиновой и при относительно высоком поле лигандов, особенно в сульфамидном комплексе, который к тому же имеет наибольшую восприимчивость. [42]
Эти модельные эксперименты дают основание думать, что карбоангидраза играет сходную роль и в биологических мембранах, например на поверхности хлоропластов. Как бы то ни было, уникальная и чрезвычайно интересная сторона такой функции карбоангидразы состоит в том, что этот фермент позволяет заряженным частицам - - НСОз - приобретать подвижность, обычно свойственную только электронейтральному газу, причем организм не теряет контроля над их концентрацией и их транспортом. [43]
После того как Манн и Кейлин [21] обнаружили ингибирова-ние карбоангидразы сульфамидами, было получено еще много подобных соединений. Установлено, что для эффективного инги-бирования структура их молекул должна удовлетворять двум общим требованиям. [44]
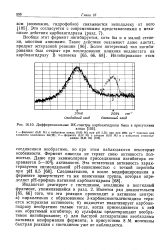 |
Дифференциальные ИК-спектры карбоангидразы быка в присутствии. [45] |
Страницы: 1 2 3 4