Амилаза - слюна
Cтраница 1
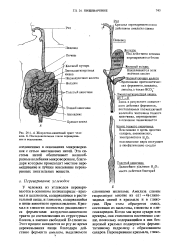 |
А. Желудочно-кишечный тракт человека. Б. Последовательные этапы переваривания и всасывания. [1] |
Амилаза слюны гидролизует многие из х ( 1 - Ч) - глико-зидных связей в крахмале и в гликогене. При этом образуется смесь, состоящая из мальтозы, глюкозы и оли-госахаридов. Когда мы жуем сухари или крекеры, они становятся постепенно слаще, поскольку содержащийся в них безвкусный крахмал подвергается ферментативному гидролизу с образованием Сахаров. [2]
Амилаза слюны является а-амилазой. [3]
Амилаза слюны, действуя на амилопектин, дает ряд резистентных разветвленных олигосахаридов. [4]
Амилаза слюны начинает свое действие в полости рта, но оно незначительно вследствие кратковременного пребывания здесь пищи. Гидролиз углеводов ферментами слюны продолжается в желудке, пока в глубокие слои его пищевого содержимого не проникает кислый желудочный сок, прекращающий действие карбогидраз и инактивирующий их. [5]
Амилаза слюны и других источников теряет способность к перевариванию крахмала ( при оптимальном рИ 6 8 этого фермента), если она диалпзована; активность возвращается при добавлении ионов хлора. Ионы брома обладают аналогичным, но более слабым эффектом; другие анионы активируют еще слабее. [6]
Для исследования активности амилазы слюны и ее свойств используют собственную слюну, разведенную в 10 раз. Для этого в мерную пробирку собирают 1 мл слюны ( предварительно полость рта споласкивают водой) и доводят водой до метки 10 мл. [7]
Важнейшим ферментом слюны является птиалин - амилаза слюны, которая катализирует гидролиз крахмала до декстринов и частично даже до мальтозы. Окончательный гидролиз этих продуктов расщепления до глюкозы осуществляется в тонком кишечнике. [8]
При пережевывании пища смешивается со слюной, и затем амилаза слюны в течение первых нескольких минут нахождения пищи в желудке вызывает превращение крахмала в мальтозу. [9]
Так, хлористый натрий в разведенных растворах ускоряет действие амилазы слюны на крахмал. Растворы сернокислой меди, наоборот, сильно замедляют действие амилазы слюны. [10]
Расщепление крахмала ( и гликогена) начинается в полости рта под действием амилазы слюны. [11]
Простым и наглядным примером, демонстрирующим действие ферментов и некоторые их свойства, является гидролиз крахмала под действием амилазы слюны. Поэтому, прежде чем перейти к изучению главнейших свойств ферментов на этом объекте, необходимо остановиться на гидролизе крахмала. [12]
Так как амилоза представляет собой легко доступный линейный а-в - ( 1 - 4) - полимер глюкозы, который при гидролизе под действием амилазы слюны превращается в мальтозу и мальтотриозу, то она является идеальным исходным материалом для получения мальтотриозы. Реакционная смесь, полученная по этому методу, не содержит сложных олигосахаридов с а-и - ( 1 - 4) - или а-в - ( 1 - 6) - связями, как это имеет место при применении некоторых других методов. Мальтоза, образующаяся из амилозы под действием амилазы слюны, удаляется ферментацией пекарскими дрожжами. Из полученного раствора мальтотриозу выделяют адсорбированием на активном угле с последующим элюированием водным спиртом. Спиртовый раствор упаривают в вакууме до сиропа. Сироп высушивают в эксикаторе и получают аморфный продукт. При хро-матографировании раствора препарата на бумаге было получено одно пятно восстанавливающего сахара, соответствующее положению три-сахарида в ряду мальтоолигосахаридов. [13]
Активность амилазы слюны выше всего при почти нейтральной реакции ( рН 6 8) и подавляется как кислотами, так и щелочами. [14]
Большинство ферментов обладает очень высокой специфичностью действия по отношению к определенным веществам ( субстратам) или определенным типам химических связей. Так, амилаза слюны расщепляет крахмал, но не действует на другой полисахарид - целлюлозу. Для осуществления взаимодействия молекул фермента и субстрата, на который воздействует фермент, нередко необходимо участие неорганических ионов. Эти ионы выступают в роли активаторов ферментов. [15]
Страницы: 1 2 3