Кинетическая длина - цепь
Cтраница 1
Кинетическая длина цепи v есть ряд мономерных молекул, используемых каждым первичным радикалом. [1]
Кинетическая длина цепи или длина зипа для термической деполимеризации, определенная из этих выражений, оказалась значительно короче, чем предполагалось. При более высоких температурах длина зипа становится короче. Хотя гипотетическая длина зипа для радиолигической деполимеризации увеличивается с уменьшением температуры, большая длина зипа имеет место только при низкой интенсивности облучения, когда деполимеризация протекает с незаметной скоростью. Малая длина зипа в сочетании с независимостью скорости разложения от молекулярного веса является очень веским доказательством того, что термическое инициирование осуществляется по закону случая. [2]
Кинетическая длина цепи / V определяется количеством превращений ( числом элементарных актов) на каждый случай инициирования цепи. Термическое разложение не является идеальным методом изучения реакций, происходящих с участием: радикалов, так как они протекают быстрее, чем первичная реакция с расщеплением связи С-С. Спорость и энергия активации всей реакции, таким образом, определяются в значительной степени первичной реакцией. Большая часть знаний о радикальных реакциях при термическом разложении углеводородов получена при изучении фотохимических и фотосенсибилизованпых реакций углеводородов, кетонов, меркуралкилов и альдегидов. В этих случаях энергия активации первичного расщепления не отражается на результатах кинетических анализов, и вся энергия активации является обычно простой функцией относительной энергии активации реакций различных радикалов. Возможно также прове дение работы при более низкой температуре, когда в значительной мере устраняется влияние побочных реакций. Таким образом, энергия активации и пространственные факторы в реакциях радикалов могут определяться независимо, ы о значении их можно судить-только по процессу чисто термического разложения. [3]
Кинетическая длина цепи ( число мономерных единиц для каждого активного конца цепи), может быть меньше, равна или больше начальной длины цепи полимера. [4]
Кинетическая длина цепи может быть определена аналитическим путем при использовании инициатора полимеризации, если удается установить число концевых групп полимера, содержащих осколки инициатора. Этот метод не зависит от того, происходит ли при обрыве цепи рекомбинация, диспропорционирование или то и другое; требуется лишь точное аналитическое определение концевых групп. Условием применимости этого метода является отсутствие сильного обрыва растущих цепей радикалами инициатора и отсутствие передачи на инициатор. Из уравнения ( 9) видно, что кинетическая длина цепи должна быть тем больше, чем ниже стационарная концентрация радикалов и соответственно скорость полимеризации. [5]
Кинетическая длина цепи соответствует данным по степени полимеризации; группы ОН, входящие в состав полимера, могут быть обнаружены инфракрасным спектральным анализом. В реакциях под действием излучения образуются аналогичные полимеры, в инфракрасных спектрах которых также обнаруживаются полосы, соответствующие группам ОН. Механизм этих реакций, в той мере, в какой он был выяснен, в сочетании с другими данными указывает на образование атомов и радикалов при действии рентгеновских и у-лучей на воду и приводит к выводу, что эти свободные атомы и радикалы распределены неравномерно по всему объему и что их местная концентрация может быть сравнительно очень высокой. [6]
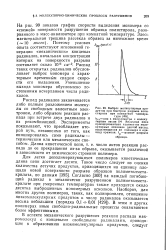 |
Выброс молекулярных продуктов при быстром разрыве полистирола при комнатной температуре 405 ]. [7] |
Для легко деполимеризующихся полимеров кинетическая длина цепи достигает десяти. Согласно [300] на каждый погибающий радикал в механически разрушенном полиметилмета-крилате при умеренных температурах также приходится около десятка выброшенных мономерных осколков. В этом и других полимерах иные свободно-радикальные процессы оказываются более эффективными. [8]
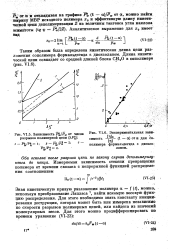 |
Зависимость P / PW от числа разрывов полимерной цепи. [9] |
Таким образом была определена Кинетическая длина цепи разложения сополимера формальдегида с диоксоланом. [10]
Суммарная скорость радикально-цепного процесса и кинетическая длина цепи, фактически определяющие выход при данных физико-химических условиях, зависят от скоростей реакций зарожде ния, развития и обрыва цепи ( см. гл. Скорость реакций зарождения цепи обычно можно регулировать подбором инициатора, температуры и других экспериментальных условий. Скорость реакций обрыва цепи не поддается прямому контролю, поэтому такие реакции являются серьезным ограничением процессов, текущих по радикально-цепному механизму. Если в течение такого короткого времени происходит большое число стадий развития цепи, то, очевидно, это является результатом малых концентраций радикалов ( их встречаТимеет значительно меньшую вероятность, чем встреча радикала и молекулы), а также результатом особенностей протекания реакций развития цепи. Количественно эти особенности, а также конкуренция между реакциями описываются на основании данных о равновесиях и константах скорости этих реакций. [11]
В большинстве радикальных цепных реакций средние кинетические длины цепей велики и, следовательно, пропорции конечных группировок, полученных из инициаторов, - очень малы. [12]
 |
Относительная реакционная способность первичных, вторичных и третичных связей С - Н при процессах радикального замещения. [13] |
Чем отрицательнее АРЯ, тем больше будет осуществляться циклов реакции, тем больше кинетическая длина цепи, и тем быстрее протекает реакция. [14]
Величина отношения полного квантового выхода к первичному ( Ф / ф) аналогична понятию кинетической длины цепи v, используемому при исследованиях термических цепных реакций. Эта величина может быть выражена также через константы скоростей вторичных реакций, и в этом случае ее изменение в зависимости от концентрации различных частиц может служить подтверждением гипотетического механизма реакции и давать оценку констант скоростей. [15]
Страницы: 1 2 3