Калиевые квасцы
Cтраница 1
Калиевые квасцы являются значительно более ценным продуктом, чем натриевые, так как в отличие от последних они путем перекристаллизации могут быть получены в очень чистом виде, что важно для многих потребителей. Поэтому раздельное получение калиевых и натриевых квасцов более рационально, чем получение смешанных квасцов путем прямой выпарки раствора. [1]
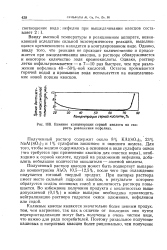 |
Влияние концентрации серной кислоты на скорость разложения нефелина. [2] |
Калиевые квасцы являются значительно более ценным продуктом, чем натриевые, так как в отличие от последних они путем перекристаллизации могут быть получены в очень чистом виде, что важно для ряда потребителей. [3]
Калиевые квасцы являются значительно более ценным продуктом, чем натриевые, так как в отличие от последних они путем перекристаллизации могут быть получены в очень чистом виде, что важно для многих потребителей. Поэтому раздельное получение калиевых и натриевых квасцов более рационально, чем получение смешанных квасцов путем прямой выпарки раствора. [4]
Дегидратация калиевых квасцов отличается от дегидратации аммониевых квасцов еще в одном важном отношении. Имеющиеся данные показывают, что при 30 скорость роста ядер при давле-нии паров воды ниже 0 1 мм рт. ст. аномально мала. [5]
Растворимость аммиачных квасцов немного менее Калиевые квасцы имеют удельный вес 1 74, аммиачные 1 63 натровые 1.60, Квасцы легко теряют свою кристаллизационную воду; так, поташные квасцы. При 100 сухой воздух, пропущенный чрез квасцы, отнимает от них почти всю воду. [6]
Как видно, растворимость калиевых квасцов резко уменьшается по мере увеличения концентрации натриевых квасцов и понижения температуры. [7]
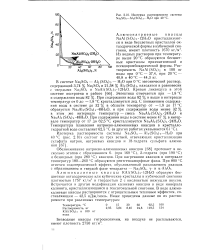 |
Изотерма растворимости системы Na2SO4 - A12 ( SO4 3 - Н2О при 40 С. [8] |
Встречается и другая модификация калиевых квасцов в виде минерала калинита, кристаллизующаяся в гексагональной сингонии. В воде алюмо-калиевые квасцы растворяются с отрицательным тепловым эффектом, составляющим - 42 5 кДж / моль. [9]
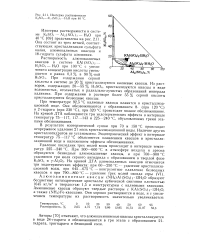 |
Изотерма растворимости KzSO-Ab ( SO. ib - Н2О При 40 С. [10] |
При температуре 92 5 С калиевые квасцы плавятся в кристаллизационной воде. Они обезвоживаются с образованием 8 - ( при 120 С) и 2-гидрата ( при 230 С), при 320 С происходит полное обезвоживание. На кривой ДТА наблюдаются три эндотермических эффекта в интервале температур 75 - 117, 117 - 143 и 225 - 240 С, обусловленных тремя этапами обезвоживания. [11]
Этой реакцией пользуются для получения хромо калиевых квасцов в промышленности. [12]
Реакция разложения нефелина серной к-той идет с образованием натриевых, калиевых квасцов и кремнекислоты. [13]
Вследствие резкого уменьшения растворимости алюмоквасцов рубидия и цезия в присутствии калиевых квасцов может быть достигнуто практически полное выделение обоих редких элементов в первичный алюмоквасцовый концентрат. Состав последнего во многом зависит от содержания щелочных элементов и алюминия в исходном сырье. При переработке алюмосиликатов типа литиевых слюд получаются концентраты, содержащие 75 - 90, 5 - 15 и 2 - 8 % квасцов калия, рубидия и цезия соответственно. [14]
Из солей хрома ( III) самой распространенной является двойная соль хрома и калия - хроме / калиевые квасцы KCr ( SO4) 2 - 12H2O, образующие сине-фиолетовые кристаллы. Хромокалиевые квасцы применяются в кожевенной промышленности для дубления кож и в текстильной промышленности в качестве протравы при крашении. [15]
Страницы: 1 2 3