Кетенимин
Cтраница 2
В обычных алифатических мононитрилах ионизация и возможность образования кетениминов выражены крайне слабо. [16]
Ряд практически осуществимых методов синтеза изоцианатов, изотиоцианатов, карбодиимидов и кетениминов основан на раскрытии цикла и фрагментации доступных гетероциклов. [17]
Основное различие между методами с применением карбо-диимидов и методами с применением кетениминов заключается в стабильности промежуточных ацилирующих соединений. [18]
Роль катализатора заключается, очевидно, в том, что он превращает электрофильный кетенимин в нуклеофильный мезомерный анион, способный присоединяться по кратной связи перфторолефина. Такое присоединение сопровождается циклизацией с генерацией катализатора. [19]
Нет ничего удивительного в том, что изоцианаты, изотиоциа-наты, карбодиимиды и кетенимины реагируют с аминосоедине-ниями ( аммиаком, первичными и вторичными аминами, гидро-ксиламинами, гидразинами) по типу 1 2-нуклеофильного присоединения. Эти реакции обычно протекают с хорошим выходом. Особенно высокую активность в реакциях этого типа проявляют кетениминиевые соли [400], дающие с очень высоким выходом амидины. [20]
Штаудингер и Мейер [42] отметили, что бензгидрилидентри-фенилфосфоран реагирует с фенилизоцианатом с образованием кетенимина, по-видимому, по механизму, подобному механизму реакции Виттига. Трипет и Уолкер [21] показали, что если илид содержит водород при илидном атоме углерода, то на стадии бетаина происходит прототропный сдвиг, причем образуется новый ацилированный илид. [21]
Существует ряд методов, позволяющих создать гетерокумуле-новые структуры изоцианатов, изотиоцианатов, карбодиимидов или кетениминов на основе превращений кратных связей, уже присутствующих в молекуле. Простейшими процессами этого типа являются реакции присоединения некоторых производных изоцианатов или изотиоцианатов к двойной углерод-углеродной связи. [22]
К числу наиболее важных реакций нуклеофильного присоединения, которым подвергаются изоцианаты, изотиоцианаты, карбодиимиды и кетенимины, относятся реакции с гидроксисоединения-ми. Карбаминовые кислоты легко отщепляют диоксид углерода, давая амины, которые, взаимодействуя с исходным изо-цианатом, образуют производные мочевины. Производные мочевины часто оказываются устойчивыми конечными продуктами реакции простых изоцианатов в водной среде, тогда как реакция ацилизоцианатов [392, 393] и сульфонилизоцианатов [391, 418] с водой останавливается на стадии образования амина, и продуктами реакции являются первичные карбоксамиды и сульфон-амиды, соответственно. Так, например, хлорсульфонилизоцианат [391, 418] превращается в водной среде в сульфамоилхлорид NH2SO2CI, являющийся превосходным реагентом для введения сульфонамидной группы в молекулу. Изотиоцианаты [344, 389], которые, в общем, не так реакционноспособны по отношению к нуклеофильным агентам, как изоцианаты, устойчивы к действию горячей воды, и для их превращения в производные тиомочевины в кислых или основных условиях требуется продолжительное нагревание. [23]
Роль такого промежуточного соединения была продемонстрирована сравнением способности инициировать полимеризацию стирола исходным азосоединением и соответствующим ему кетенимином. [24]
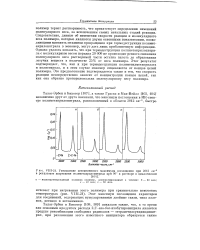 |
Уменьшение кетениминного максимума поглощения при 2012 см - в результате нагревания полиметакрилонитрила при 90 в растворе в циклогексане. [25] |
Этот максимум поглощения характерен для соединений, содержащих кумулированные двойные связи, типа алле-нов, кетенов и кетениминов. [26]
Смесь нагревают с обратным холодильником до кипения в течение 1 час 40 мин, хотя желтая окраска кетенимина полностью исчезает уже через 15 мин. [27]
Очевидно, что реакция ( в) выгоднее перегруппировки Вольфа, так как в этом случае не образуются кетенимины. [28]
При взаимодействии р р р-триалкилпропионитрилов с алКилга - логенидами в присутствии амида натрия наряду с а-моно - и а а-ди-алкилнитрилами в качестве побочных продуктов образуются N-за-мещенные кетенимины. [29]
Карбоциклы 205 N-Карбэтоксиазиридин 158 Карбэтоксиамидины 52 а - Карбэтокси - Р - аминоакрилонитрил 149 о - Карбэтоксифенилацетонитрил 238 2 - Карбэтокси-2 - этилбутиронитрил 105 Каучук натуральный 265 о - Кетамиды 297 Кетенимины 15 ел. [30]
Страницы: 1 2 3