Килпатрик
Cтраница 3
Способом организации такой деятельности должен был служить, в частности, разработанный учеником и последователем Д, Дьюи, американским педагогом, видным представителем прогрессивизма Уильямом Килпатриком ( 1871 - 1965) метод проектов. Согласно ему обучение осуществляется через организацию целевых актов. Дети в процессе учебной деятельности планируют ( проектируют) выполнение конкретной практической задачи, включая туда и учебную деятельность. [31]
Обширные исследования относительной силы кислот, растворенных в бутиловом спирте, были выполнены Уотеном и Хамметом [ 74а ] с помощью электрометрического метода, а также Мэзоном и Килпатриком [746], применившими фотоэлектрический колориметр. [32]
Обширные исследования относительной силы кислот, растворенных в бутиловом спирте, были выполнены Уотсном и Хамметом [ 74а ] с помощью электрометрического метода, а также Мэзопом и Килпатриком [746], применившими фотоэлектрический колориметр. [33]
Впоследствии было найдено, что трехфтористый бор играет ту же роль. Килпатрик и Любарский [39], измерив электропроводность таких растворов, определили константы ионизации углеводородных оснований и тем самым показали, что эти растворы содержат ионы. Трехфтористый бор значительно увеличивает электропроводность при соотношении 1 моль на 1 моль основания, но для тех соединений, электропроводность которых велика, трехфтористый бор не способствует дальнейшей ионизации. При этом электропроводность даже до некоторой степени уменьшается, но не из-за уменьшения числа ионов, а вследствие меньшей подвижности BFj-иона по сравнению с фтор-ионом. В этих растворах происходит полная ионизация, однако в случае менее основных бензола или толуола при взаимодействии с фтористым водородом образуется только небольшое число ионов. Браун и Нельсон [19] предположили, что менее основные углеводороды образуют я-комплексы ArH-HF, в то время как более основные образуют т-комплексы. Этот вывод представляется весьма важным, поскольку он предполагает, что разделение между я - и а-комплексами не такое резкое и что между ними имеется постепенный переход, который зависит как от электрофильности акцептора, так и от основности донора. [34]
Килпатрика, содержит оригинальные задачи повышенной трудности по элементарной математике, которые предлагались американским школьникам на протяжении ряда лет иа конкурсах в Стэифордском. [35]
Так, Эллиот и Килпатрик [105] отмечали, что линейная зависимость между логарифмом констант диссоциации бензойных кислот в водном ди-оксане и 1 / е наблюдается лишь в области е 25, а в менее полярных средах становится существенной специфическая сольватация. Наличие специфической сольватации приводит к неудовлетворительной корреляции между р и 1 / е в реакции замещенных а-хлор-толуолов с тиосульфатом [106], изученной весьма основательно в ряде растворителей различной природы и полярности. Такой случай описан в одной из работ авторов [108], посвященной механизму взаимодействия изоцианатов со спиртами. [36]
Этиленовые двойные связи с гранс-расположением заместителей дают полосу при 990 - 965 см-1, интенсивность которой изменяется от средней до более высокой. Эта полоса, как было показано Килпатриком и Питцером [35], обусловлена деформационными колебаниями атомов водорода, при которых последние выходят из плоскости двойной связи. Вследствие этого изменение массы любого из заместителей при атомах углерода очень мало влияет на положение полосы, а интенсивность уменьшается при увеличении молекулярного веса и обратно. Это объясняется тем, что абсолютная интенсивность полосы на каждую двойную связь есть величина постоянная, а количество двойных связей на единицу объема вещества при увеличении длины цепи уменьшается. Расмуссен и Браттен [33] показали, что эта полоса поглощения появляется только при гране-конфигурации молекул, что служит ценным указанием при выяснении вопросов цис - и транс-изомерии. [37]
Авторы этого сообщения делают критические замечания в адрес Даффи и Килпатрика и Спитцера ( последние заслужили упрек за введение некоторых предположений ad hoc), но не упоминают о гипотезе Уолша, с которой они, по-видимому, еще не были знакомы, Коулсон и Моффит кратко излагают свой подход к вопросу о нетет-раэдрическом углеродном атоме с напряженными связями на примере циклопропана. [38]
Дункан и Янц [357] произвели отнесения основных частот и рассчитали термодинамические функции, приняв потенциальный барьер внутреннего вращения равным 5 2 ккал / молъ. Проверка этих расчетов приводит к значению 5 98 ( g) 67 61 кал / ( жоль - К), если пользоватьея параметрами Дункана и Янца, и к значению S 9S ( g) 68 24 кеи / ( л оль - К), если принять параметры Вебера и Килпатрика. Причина таких расхождений не выяснена. Для наших целей мы приняли значение S MS ( g) 68 50 кал / ( молъ - К), которое получается при сочетании величины потенциального барьера 2500 кал / моль с отнесениями Дункана и Янца. Теплоемкости рассчитаны также с учетом этих отнесений и указанной величины барьера. [39]
Килпатрик, воспитание может превратиться в непрерывную перестройку жизни ребенка и поднять ее на высшую ступень, а школа будет готовить учащихся к условиям динамично меняющейся обстановки в обществе и к столкновению с неизвестными проблемами в будущем. [40]
Приведенные выше таблицы применимы и здесь. Позднее Килпатрик и Питцер [752] предложили методику расчета термодинамических функций для общего случая одного или нескольких волчков любой симметрии. Астон [31] рассмотрел методики расчета для молекул, обладающих некоторой разностью энергии между вращающимися изомерами. Скотт и Мак-Каллох [1317] предложили таблицы таких вкладов в термодинамические функции для ряда изомеров. [41]
Приведенные выше таблицы применимы и здесь. Позднее Килпатрик и Питцер [752] предложили методику расчета термодинамических функций для общего случая одного или нескольких волчков любой симметрии. Астон [31] рассмотрел методики расчета для молекул, обладающих некоторой разностью энергии между вращающимися изомерами. Скотт и Мак-Каллох [1317] предложили таблицы таких вкладов в термодинамические функции для ряда изомеров. [42]
Однако при таком механизме общекислотный катализ и большой изотопный эффект растворителя могут наблюдаться и для других олефинов, поскольку стадия, определяющая скорости реакции, в данном случае в меньшей степени отличается от той же стадии в случае присоединения к простым олефинам, чем это предполагалось ранее. В связи с этим стоит напомнить, что Чапетта и Килпатрик [22] заметили, что присоединение воды к изобутилену в присутствии три-хлоруксусной кислоты происходит быстрее, чем можно ожидать при значениях рН, соответствующих высоким концентрациям катализатора. [43]
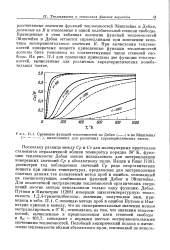 |
Сравнение функций теплоемкостей по Дебаю ( - - - - - и по Эйнштейну. [44] |
Поскольку разница между Ср и Си для молекулярных кристаллов становится неразличимой вблизи температур порядка 30 К, функцию теплоемкости Дебая можно использовать для экстраполяции измеренных значений Ср к абсолютному нулю. Путнам и Килпатрик [1208] измерили низкотемпературную теплоемкость 1 2 4-триметилбензола; значения, полученные ими, приведены в табл. II.1. С помощью метода проб и ошибок Путнам и Килпатрик пришли к выводу, что их экспериментальные значения можно экстраполировать к 0 К, основываясь на том, что значения теплоемкостей, вычисленные в предположении пяти степеней свободы и 6Л 103 7, совпадают с первыми шестью экспериментальными значениями теплоемкостей. [45]
Страницы: 1 2 3 4