Кинетика - окисление
Cтраница 1
Кинетика окисления этих сплавов полностью отличается от сплавов, рассмотренных до сих пор. Сплав А3 показал результаты, подобные тем, которые получены для чистого сплава нихром 80 / 20: за 1000 час. [1]
Кинетика окисления изучалась методом периодического взвешивания на установке, позволяющей проводить одновременное исследование шести образцов, не прерывая процесса окисления. [2]
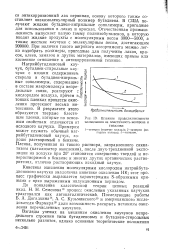 |
Влияние продолжительности. [3] |
Кинетика окисления молекулярным кислородом натрийбута-диенового каучука аналогична кинетике окисления НК; этот процесс графически выражается характерными S-образными кривыми с ярко выраженным индукционным периодом. [4]
Кинетика окисления и структура окислов некоторых промышленных жаростойких сталей и сплавов: Сборник / / Исследование по жаропрочным сплавам. [5]
Кинетика окисления этого сплава при 900 на воздухе опреде - ляется параболическим уравнением, в печной атмосфере при а 0 8 и 1 5 - логарифмическим уравнением. [6]
Кинетика окисления некоторых сплавов сопротивления в цементационной атмосфере приведена на фиг. [7]
Кинетика окисления флуорена и аценафтена в водно-щелочной среде. В настоящее время не существует единой физической модели, на основе которой можно было бы хотя бы приблизительно определить скорость гетерогенных реакций. [8]
Кинетика окисления СО на чистом палладии изучена в работе [ 22, с. В кинетической области реакция характеризуется энергией активации 54 кДж / моль. [9]
Кинетика окисления фосфина в адсорбированном слое при 18 может быть представлена уравнением Рогинского, справедливым для поверхностей, равномерно неоднородных по энергиям активации процесса адсорбции. [10]
Кинетика окисления галоидолефинов изучена мало. В настоящем сообщении приведены результаты исследования кинетики низкотемпературного жидкофазного окисления тетра - и трихлорэтиленов. Окисление тетра-хлорэтилена проводили при 60 - - 120 С, а трихлорэтилена - при 30 -: - 70 С, пропуская кислород через 100 мл тетрахлорэтилена со скоростью 0 3 л / мин, а трихлорэтилена - 0 4 л / мин. [11]
Кинетика окисления поликарбоната характеризуется наличием периода индукции. Начальная скорость реакции пропорциональна давлению кислорода. Энергия активации составляет 36 5 ккал / моль. В газообразных продуктах реакции содержится значительное количество СО, ССЬ, следы На, а также вода и НСНО. [12]
Кинетика окисления углерода до сих пор полностью непонята. [13]
Кинетика окисления аммиака воздухом, обогащенным кислородом, Журн. [14]
Кинетика окисления м-бутана или изобутана при низком давлении настолько подобна окислению пропана, что этот вопрос не требует детального обсуждения. [15]
Страницы: 1 2 3 4 5