Кинетика - окисление
Cтраница 3
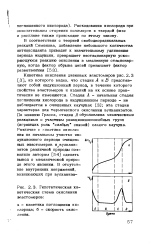 |
Гипотетическая кинетическая схема окисления эластомеров. [31] |
Кинетика окисления диеновых эластомеров рис. 2.3 ЦЗ ], из которого видно, что стадии А и В представляют собой индукционный период, в течение которого свойства эластомеров и изделий на их основе практически не изменяются. Стадия А - начальная стадия поглощения кислорода в индукционном периоде - не наблюдается в очищенных каучуках [3]; эта стадия характерна для термического окисления вулканизатов. По мнению Грасси, стадия А обусловлена химическими реакциями с участием реакционноспособных групп ( играющих роль слабых связей) самого каучука. [32]
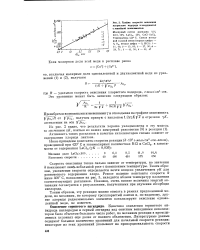 |
График скорости окисления хлористого водорода в координатах с линейной зависимостью. [33] |
Кинетика окисления сернистого ангидрида кислородом в серный ангидрид над окисным ванадиевым катализатором была объектом большого числа работ, но механизм реакции в промышленных условиях еще далек от полного объяснения. [34]
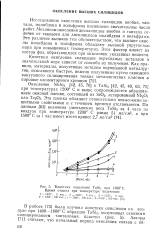 |
Кинетика окисления TaSia при 1500 С. Время отжига при температуре получения. [35] |
Кинетика окисления силицидов переходных металлов в значительной мере зависит от способа их получения. [36]
Кинетика окисления группы хромистых сталей на воздухе при 900 и 1100 в сравнении с железом приведена на фиг. [37]
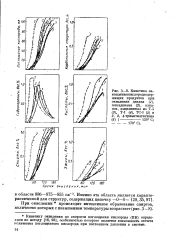 |
Кинетика на-коплениякислородсодер-жащих продуктов при окислении декана ( 1, гексадекана ( 2, алка-нов, выделенных из Т-5 ( 3, Т-1 ( 4, ТС-1 ( 5 и 2, 2, 4-триметилгептана. [38] |
Кинетику окисления по скорости поглощения кислорода ( ПК) определяли по методу 16, 98 ], особенностью которого является возможность отсчета количества поглощенного кислорода при постоянном давлении в системе. [39]
Кинетику окисления периодата см. Strickland J.D. H. Реакция окисления сложная, природа реакции автокаталитическая. [40]
Кинетику окисления хинолфосфатов и их реакционную способность исследовали на примере 2 3-диметил - 1 4-нафтохинол - 1-диметилфосфата и 2 3-дихлор - 1 4-нафт-охинол - 1-диметилфосфата. [42]
Исследована кинетика окисления кислородом двух субстратов неорганического феррицианид-иона и органического соединения гидрохинона. При этом изучена зависимость скорости гомогенного окисления в растворе от концентрации фермента, субстратов, ионов водорода. [43]
 |
Рисунков 5. Библиографических ссылок 8.| Рисунков 3. Библиографических ссылок 7. [44] |
Изучена кинетика окисления при различных условиях. Определена скорость окисления при постоянной концентрации ТБЭ и меняющейся концентрации металлов, и наоборот. В обоих случаях получена похожая зависимость скорость окисления как от концентрации ТБЭ, так и от концентрации стеаратов металлов. Зависимость имеет вид кривой насыщения. Это объяснено взаимным влиянием Т Б Э и солей металлов друг на друга. Предполагается, что ТБЭ активирует металл в реакции инициирования цепей. [45]
Страницы: 1 2 3 4 5
