Кинетика - поглощение - кислород
Cтраница 1
 |
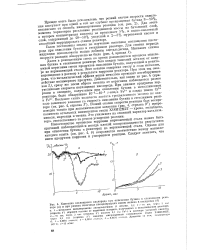
Кинетика окисления топлива Т-6 растворенным кислородом в замкнутом объеме. [1] |
Кинетика поглощения кислорода и образования продуктов окисления для топлива Т-6 при 130 С показана на рис. 4.6. Растворенный кислород окисляет топливо с образованием спиртов, карбонильных соединений и кислот. Характер кинетических кривых продуктов окисления указывает на то, что гидроперок-сиды, спирты и карбонильные соединения являются промежуточными соединениями. Концентрация каждого продукта в ходе опыта проходит через максимум, но максимумы смещены относительно друг друга во времени. [2]
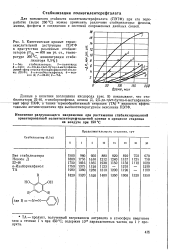
Исследования кинетики поглощения кислорода ( рис. 6), потерь массы ( рис. 7) и изменения характеристической вязкости ( рис. 8) при ингибирован-ном термоокислении поликарбоната показывают, что такие соединения с сопряженными двойными связями, как продукты взаимодействия антрацена с серой и полихинондиоксины, а также фосфорсодержащие антиоксиданты ( полигард или 2 б-ди-грег-бутил - 4-метилфенилрвый эфир пирокатехинфосфор истой кислоты) являются весьма эффективными высокотемпературными стабилизаторами для поликарбоната. [3]
Сравним кинетику поглощения кислорода в присутствии ингибитора, разрушающего гидроперекись, и без него. [4]
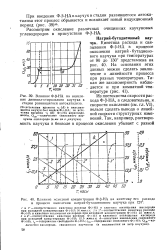 |
Влияние Ф - ( 3 - НА на окисление дивинил-стирольного каучука в.| Влияние исходной концентрации Ф - ( 3 - НА на кинетику его расхода в процессе окисления натрий-бутадиенового каучука при 120. [5] |
НА и кинетика поглощения кислорода при исходной концентрации Ф - З - НА 12 5 ммол: л; 4 - кинетика накопления связанного Ф - З - НА. [6]
 |
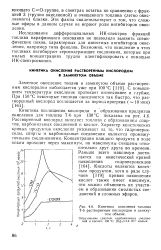
Кинетика уменьшения давления АР ( Ро. 240 103 Па при термоокислительной деструкции поликарбонатов при 300 С ( а и. [7] |
При изучении кинетики поглощения кислорода при термоокислении поликарбонатов было установлено, что, как и следовало ожидать, поликарбонаты, содержащие третичный атом углерода ( ПК-3 и ПК-4), нестабильны; их окисление начинается уже при 160 С. [8]
 |
Кинетические кривые термоокислительной деструкции ПЭТФ в присутствии различных стабилизаторов ( РОз 400 мм рт. ст., температура 260 С, концентрация стабилизатора 0 5 %. [9] |
Данные о кинетике поглощения кислорода ( рис. 5) показывают, что стабилизаторы 22 - 46, ге-изоборнилфенол, неозон Д, 2 5-ди-тре Г бутил-4 - метилфенило-вый зфир ПКФ, а также чермоибработанный антрацен ( ТА) являются эффек-тивными антиоксидантами при высокотемпературном окислении ПЭТФ. [10]
Таким образом, исследование кинетики поглощения кислорода и роста оптической плотности окисленных образцов свидетельствует о снижении термоокислительной стабильности дизельных топ лив с ростом глубины гидроочистки. При переходе от топлив с умеренным содержанием серы ( 0.10 % масс, серы) к малосернистым топливам ( 0.02 % масс, серы) наблюдается существенное сокращение начального периода окисления tmax от 60 до 20 мин, характеризующегося незначительным ростом оптической плотности, связанной со смолообразованием в системе. Далее процесс переходит в режим максимальной скорости окисления, сопровождающийся резким увеличением оптической плотности топлива. [12]
Были поставлены опыты по изучению кинетики поглощения кислорода при окислении бутана в стеклянном реакторе. [14]
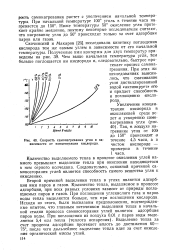 |
Скорость самонагревания угля в за - течение 4 5 часа, а в висимости от концентрации кислорода. ЧИСТОМ кислороде. [15] |
Страницы: 1 2 3 4 5