Кинетика - суммарный процесс
Cтраница 1
Кинетика суммарного процесса иослвдовалас параллельно химический и электроки-нетическим методом, что позволило установить идентичность получаемых по обоим методам результатов и сравнить скорость отверждения модельной смеси со скоростью отверждения эпоксидной еиолы. [1]
Если кинетика суммарного процесса не определялась, распределение реагента во времени показывает только, являются ли реакции однотипными, без уточнения их формы. [2]
 |
Параметры Q и е. [3] |
В кинетике суммарного процесса полимеризации двух мономеров имеются осложнения, вызванные увеличением числа элементарных актов по сравнению с гомополимеризацией. [4]
 |
Скорость этерификации уксусной кислоты ( ва катионите КУ-2. [5] |
Вклад диффузионных торможений в кинетику суммарного процесса может для одной и той же реакции варьировать в широких пределах, в зависимости от условий ее проведения. В этом отношении весьма показательны данные исследования кинетики этерификации уксусной кислоты этиловым спиртом в парообразной76 и жидкой77 фазах. [6]
Метод стационарных концентраций применим, если при рассмотрении кинетики суммарного процесса можно пренебречь временем установления стационарной концентрации активных промежуточных частиц. [7]
Химическая реакция может оказывать влияние не только на кинетику суммарного процесса, но и на скорость его электрохимических стадий при том условии, что химические превращения осуществляются на поверхности электрода или в приэлектродном слое раствора. [8]
Отсюда, в частности, следует, что, изучая кинетику суммарного процесса, можно определить формулу того активированного комплекса, который определяет скорость всей реакции. Если скорость реакций между А и В определяется произведением с. Иногда оказывается, что наблюдаемый порядок реакции значительно меньше требуемого стехиометрическим уравнением. Особенно часто такое явление наблюдается для сложных реакций, которые, несомненно, протекают в несколько стадий. Это означает, что в стадии, определяющей скорость реакции, участвует небольшое число молекул и соответствующий активированный комплекс должен быть относительно простым. [9]
Скорости ионных реакций в растворе обычно весьма значительны, и поэтому кинетику суммарного процесса будет определять замедленность стадии разряда органической молекулы. [10]
Скорости ионных реакций в растворе обычно весьма значительны, и поэтому кинетику суммарного процесса будет определять замедленность первой стадии разряда органической молекулы. [11]
Скорости ионных реакций в растворе обычно весьма значительны, и поэтому кинетику суммарного процесса будет определять замедленность стадии разряда органической молекулы. [12]
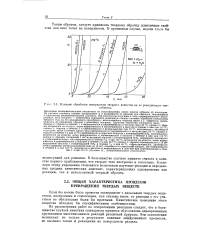 |
Влияние обработки поверхности твердого вещества на ее реакционную способность. [13] |
Из рассмотрения работ по гетерогенным реакциям следует, что в большинстве случаев кинетика суммарного процесса обусловлена одновременным протеканием многочисленных реакций различной природы. Эти осложнения возникают не только в результате влияния диффузионных процессов, но вызваны также и реакциями на поверхности раздела. [14]
Если наиболее медленным звеном процесса является подвод реагирующих веществ к зоне реакции или отвод из нее продуктов реакции, то кинетика суммарного процесса будет диффузионной. [15]
Страницы: 1 2 3