Кинетика - фотохимическая реакция
Cтраница 2
Следовательно, макрокинетика процесса фотоокисления пленок полипропилена существенно отличается от кинетики простых фотохимических реакций. Несмотря на то, что в данном случае фотоокисление обусловлено классической одноквантовой фотореакцией распада пе-роксида, процесс разрушения полипропилена не может быть описан как классическая фотохимическая реакция. [16]
Метод стационарных концентраций был впервые с успехом использован при изучении кинетики фотохимических реакций в газах [1], а сейчас применяется почти всегда при исследованиях механизмов радиолитических превращений. [17]
Недооценка роли этого фактора часто приводит к неправильным заключениям о кинетике фотохимических реакций, так же как и к неверным выводам о тушащем действии тех или иных газов ( см. [ 175, стр. [18]
В 1904 г. Вант-Гофф сформулировал количественную закономерность, лежащую в основе кинетики фотохимических реакций: количество фотохимически измененного вещества пропорционально поглощенной энергии света. [19]
В 1904 г. Вант-Гофф формулировал количественную закономерность, лежащую в основе кинетики фотохимических реакций: количество фотохимически измененного вещества пропорционально поглощенной энергии света. [20]
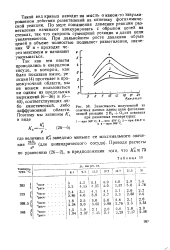 |
Зависимость полученной из опытных данных длины цепи фотохимической реакции 2 Н2 - - О2 от давления при различных температурах. [21] |
Такой вид кривых наводит на мысль о каком-то завуалированном действии разветвлений на кинетику фотохимической реакции. По мере повышения давления реакции разветвления начинают конкурировать с обрывом цепей на стенках, так что скорость суммарной реакции и длина цепи увеличиваются. При дальнейшем росте давления обрыв цепей в объеме полностью подавляет разветвления, значения W и v проходят через максимум и начинают уменьшаться. [22]
Кистяковский совместно с Ван-Артсдаленом и другими [1, 20, 23] измерили энергию диссоциации некоторых соединений на основе детального изучения кинетики фотохимической реакции бронирования углеводородов. [23]
За поглощением молекулой света следуют параллельные и последовательные физические и химические процессы, сложное соотношение которых определяет кинетику фотохимической реакции. Поэтому целесообразно сначала рассмотреть кинетические закономерности отдельно физических и химических процессов. [24]
 |
Установка Для облучения при низких температурах ( до - 170 С. [25] |
Другие требования являются исходными при разработке аппаратов для физических измерений и соответствующих методов работы. Они предназначены для определения квантовых выходов и исследования кинетики фотохимических реакций. Поэтому необходимо проводить точное измерение интенсивности поглощаемого света и продолжительности реакции, а также точное ( непрерывное) определение концентраций участвующих в фотореакции веществ. Это относительно просто, если соблюдаются условия, указанные в разделе 5.3. Кроме того, должен быть возможен точный и, желательно, непрерывный контроль концентраций участвующих в реакции веществ. Для этого особенно удобны спектрофотомет-рические методы. [26]
Недооценка роли этого фактора часто приводит к неправильным заключениям о кинетике фотохимических реакций, так же как и к неверным выводам о тушащем действии тех или иных газов. Так, например, на основании правильного учета изменения поглощения света в результате ударного уширения линий поглощения было показано [191], что обнаруженное Стюартом [1190] тушение резонансной флуоресценции ртути гелием и аргоном, так же как и наблюдавшееся Мэннкопфом [910,604] тушение резонансной флуоресценции натрия смесью гелия и неона, целиком обусловлено изменением поглощения возбуждающего света и, следовательно, не имеет ничего общего с истинным тушением флуоресценции. [27]
В книге выведены и обсуждены на основе примеров различные уравнения и методы химической кинетики в газах и растворах. Критически рассмотрены основные теории: теория активных столкновений, теория переходного состояния и теория цепных реакций. Отдельные главы посвящены кинетике фотохимических реакций, реакций в электрических разрядах и сверхбыстрых реакций в растворах. [28]
Механизм этих реакций может быть весьма сложен. Решающим шагом в разработке кинетики фотохимических реакций является открытие Эйнштейном закона фотохимического эквивалента. Согласно этому закону каждый квант света при поглощении его веществом вызывает один элементарный акт химической реакции. [29]
При непрерывном облучении возбужденные состояния оказываются в некоторых малых квазистационарных концентрациях. Поэтому к решению систем соответствующих кинетических уравнений применим принцип Боденштейна. В форме уравнения Штерна - Фольмера (5.19) он играет важную роль в описании кинетики фотохимических реакций. [30]
Страницы: 1 2 3