Кинетика - гомогенная реакция
Cтраница 3
В книге представлены теплофизические и теплохимические характеристики газов, промышленная классификация газообразного топлива, дано обобщение экспериментальных и теоретических исследований механизма и кинетики гомогенных реакций горения метана, формальдегида, окиси углерода. Рассматриваются результаты экспериментальных и теоретических исследований в области горения углерода, впервые приводится материал по цепному реагированию углерода. [31]
Так как отношению W / F можно приписать размерность времени, оно часто обозначается как время контакта или время пребывания по аналогии с кинетикой гомогенных реакций. [32]
В связи с очень низкой концентрацией ( активностью) электронов в объеме раствора скорости прямой и обратной реакции вида (1.1) в растворе столь незначительны, что при обсуждении кинетики гомогенных реакций их не учитывают. [33]
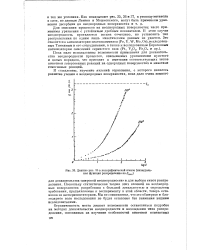 |
Данные 35 в логарифмической шкале ( интегральная функция распределении по Еклт. [34] |
Пока мало использованы возможности применения для доказательства неоднородности процессов, описываемых уравнениями нулевого и целых порядков, что приводит к имитации соответствующих типов кинетики гетерогенных реакций на однородных поверхностях и кинетики гомогенных реакций. [35]
В области кинетики гетерогенных реакций, как правило, оценка констант в математических выражениях затруднена, за исключением случая, когда анаморфозы кривых приводят к простому графическому определению этих констант, вопреки тому что часто бываете кинетике гомогенных реакций. [36]
Влияние стенок на газо - и жидкофазные некаталитические реакции. Как известно, кинетика газофазных гомогенных реакций в большей или меньшей степени зависит от природы и состояния стенок реакторов; специальная обработка стенок различными реагентами или тренировка их реакцией устанавливает постоянство их влияния на протекающие в их присутствии процессы, но не ликвидирует его. [37]
Число столкновений должно увеличиваться с повышением концентрации реагирующих веществ. Для наиболее простых по кинетике гомогенных реакций опыт показывает, что при постоянной температуре скорость данной реакции прямо пропорциональна произведению концентраций реагирующих веществ, причем каждая из концентраций участвует в степени, в простейших случаях равной коэффициенту перед форму. [38]
К числу безградиентных реакторов, не содержащих движущихся частей, относятся и аппараты, в которых полное смешение достигается благодаря приданию им специальной формы [32], а также вследствие энергии потока газовой смеси, тангенциально вводимой в аппарат. Такой кварцевый реактор применялся [33] для исследования в лабораторных условиях кинетики гомогенных реакций при температурах 900 - 1100 С; он представлял собой цилиндрический тороид, образованный двумя спаянными сосудами с цилиндрическими днищами. [39]
Другие соотношения в уравнениях скорости, выраженные через концентрации С, парциальные давления р и мольные доли N, например выражения для таких производных, как dp / dt и dNIdt, описаны ниже ( см. стр. Уравнения, представленные в табл. 1, являются основными при изучении кинетики гомогенных реакций. [40]
Другие соотношения в уравнениях скорости, выраженные через концентрации С, парциальные давления р и мольные доли N, например выражения для таких производных, как dp / dt и dN / dt, описаны ниже ( см. стр. Уравнения, представленные в табл. 1, являются основными при изучении кинетики гомогенных реакций. [41]
Другие соотношения в уравнениях скорости, выраженные через концентрации С, парциальные давления р и мольные доли Л, например выражения для таких производных, как dp / dt и dN / dt, описаны ниже ( см. стр. Уравнения, представленные в табл. 1, являются основными при изучении кинетики гомогенных реакций. В последующих главах поясняется их применение и составление по экспериментальным кинетическим данным той или иной конкретней реакции. Применение уравнения скорости для расчета показано в следующем примере. [42]
Другие соотношения в уравнениях скорости, выраженные через концентрации С, парциальные давления р и мольные доли N, например выражения для таких производных, как dp / dt и dN / dt, описаны ниже ( см. стр. Уравнения, представленные в табл. 1, являются основными при изучении кинетики гомогенных реакций. В последующих главах поясняется их применение и составление по экспериментальным кинетическим данным той или иной конкретной реакции. Применение уравнения скорости для расчета показано в следующем примере. [43]
 |
Примеры наложений активированного комплекса на поверхности для разных граней кристаллической решетки никеля. ( ПО. g - 2. ( 100. g4. ( 111. g6. [44] |
Смысл каждой из этих констант, характеризующих скорость элементарных стадий, может быть вскрыт методом переходного состояния. В I главе были изложены общие черты этого метода в применении к кинетике гомогенных реакций. [45]
Страницы: 1 2 3 4