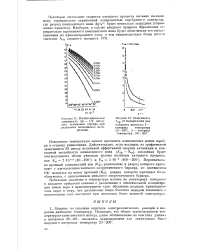
Кинетика - электрохимическая реакция
Cтраница 1
 |
Токи обмена и коэффициенты переноса электродных реакций в расплавах. [1] |
Кинетика электрохимических реакций в твердых электролитах зависит от обратимости электрода по отношению к определенным ионам твердого электролита. Характерной особенностью диффузии в твердых электролитах является то, что перенос осуществляется одним сортом ионов. Поэтому, если электрод обратим относительно основных носителей, то, ввиду их высокой концентрации, Диффузионные затруднения обычно малы и скорость реакции определяется электрохимической стадией. Анодная поляризация такого электрода включает концентрационную поляризацию, которая повышается при замене амальгамы на серебро, что связано с уменьшением поверхности контакта. [2]
Обычно кинетика электрохимических реакций изучается на выборочных и наиболее простых электродных реакциях. [3]
Изучение кинетики электрохимических реакций показывает, что реальные процессы на электродах состоят из ряда диффузи онных, химических и электрохимических стадий. [4]
Развитие кинетики электрохимических реакций в последние годы ознаменовалось началом систематического изучения таких экектрод-ных реакций, протекание которых тесно связано с сопутствующими химическими реакциями в объеме раствора. [5]
Изучение кинетики электрохимических реакций проводят методом поляризационных измерений. При помощи потенциомет-рически включенного реостата 2 на электроды подают определенное напряжение, измеряемое вольтметром 3; амперметром 4 измеряют силу тока. Электролизером 10 служит трехэлектродная электрохимическая ячейка с рубашкой для термостатирования. Измерительный контур представляет собой потенциометрическую схему 6, или потенциометр. Исследования ведут в интервале температур 20 - 80 С. [6]
Изучение кинетики электрохимических реакций показывает, что реальные процессы на электродах состоят из ряда диффузионных, химических и электрохимических стадий. [7]
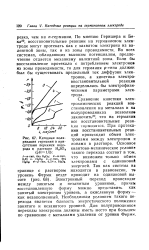 |
Катодная поляризация германия в присутствии перекиси водорода в растворе H2SO4 ( рН1 0. [8] |
Сравнение кинетики электрохимических реакций вое-сгановления на металлах и на полупроводниках позволил заключить20, что на германии все восстановительные реакции тормозятся. При протекании восстановительных реакций происходит обмен электронами между электродом и ионами в растворе. Основное квантово-механическое условие такого перехода состоит в том. [9]
Описать кинетику электрохимических реакций, когда 9 1 и лимитирующей является стадия разряда - ионизации, можно, предполагая, что адсорбция ПАОВ описывается обобщенной изотермой Фрумкина (2.46), а активированный комплекс образуется замещением адсорбированных молекул ПАОВ или растворителя. [10]
Впервые исследована кинетика электрохимических реакций в широком диапазоне температур. [12]
Для исследования кинетики электрохимических реакций в последнее время успешно используют потенциостатические, гальваностатические и переменноточные методы. Эти методы подробно описаны в недавно вышедшей книге Дамаскина [59] и поэтому здесь рассматриваться не будут. [13]
При исследовании кинетики электрохимических реакций, скорость которых значительна, применяют метод переменного тока с целью устранения диффузионных ограничений. При этом двойной электрический слой уподобляют омическому и емкостному сопротивлениям, которые измеряются путем сравнения с эталонами емкостного и vомического сопротивления. В наиболее простом случае двойной слой представляют как последовательно соединенные омические и емкостные сопротивления. [14]
При изучении кинетики электрохимических реакций имеет большое значение исследование кривых потенциал - время. Изменение поляризации во времени при постоянной величине тока позволяет судить об интенсивности разрастания образующегося на катоде осадка. Снятие кривых потенциал - время позволяет оценить эффект действия плотности тока, поверхностно активных веществ, вводимых в электролит, и других параметров на микроструктуру катодных осадков. [15]
Страницы: 1 2 3 4