Кинетика - электрохимическая реакция
Cтраница 4
Методы переменнотоковой вольтамперометрии широко используют для исследования кинетики различных электрохимических реакций. Она может быть увеличена примерно на порядок, если использовать разновидности этих методов, в которых фиксируется переменнотоковый сигнал не основной частоты переменного напряжения, а второй ее гармоники или основанные на еще более сложных явлениях. [46]
 |
Влияние ингибиторов на ход поляризационных кривых в растворе электролита. [47] |
Изменяя скорость коррозии, ингибиторы влияют на кинетику электрохимических реакций. [48]
Отмечено, что теоретическое решение задачи о кинетике электрохимических реакций в потоке требует дальнейшей разработки. [49]
Вопрос о применении капельного ртутного электрода для изучения кинетики электрохимических реакций требует некоторого пояснения. Как известно, такой электрод часто применяется в разнообразных электрохимических исследованиях, являясь основой широко распространенного метода полярографического анализа. Эта теория, развитая в свое время Илько-вичем [8], не может быть распространена на необратимые реакции. Для того чтобы при изучении указанных выше реакций все же иметь возможность воспользоваться всеми преимуществами капельного электрода, необходимо было подвергнуть анализу условия, возникающие на его поверхности при течении необратимой реакции. [50]
При анализе возможного влияния адсорбированных поверхностно-активных веществ на кинетику электрохимических реакций и коррозию следует также учитывать характер коррозионной среды. Выведенные выше уравнения справедливы лишь для кислых сред. В нейтральных же и щелочных средах, в которых разряд водорода происходит из молекул воды, г н-потенциал, определяющий скорость этой реакции, будет иметь обратный знак и, следовательно, ожидаемые закономерности будут иными. [51]
В настоящее время накоплен обширный экспериментальный материал по кинетике электрохимических реакций в области высоких заполнений поверхности электрода ПАОВ. Однако для интерпретации кинетических закономерностей на электродах, практически полностью покрытых ПАОВ, разные авторы привлекают различные механизмы. [52]
Сила тока в любой точке полярографической волны определяется кинетикой электрохимической реакции и скоростью транспортировки вещества, участвующего в электродном процессе. [53]
Ток при необходимом значетш потенциала электрода ПИП определяется кинетикой электрохимической реакции и скоростью переноса А. [54]
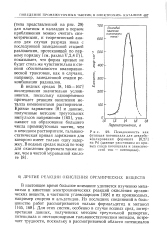 |
Псевдоемкость как функция потенциала для декарбо-ксилирования формиата на РА ( данные рассчитаны из кривых спада потенциала и зависимостей ток - потенциал. [55] |
В настоящее время большое внимание уделяется изучению механизма и кинетики электрохимических реакций окисления органических веществ, в частности углеводородов [168] и их производных, например спиртов и альдегидов. [56]
Необходимость разделения поляризационных кривых особенно велика в случае изучения кинетики электрохимических реакций при электроосаждении сплава на катоде. [57]
Приведенная или ф-шкала потенциалов и ее использование при изучении кинетики электрохимических реакций. [58]
Тормозящее действие любых ингибиторов коррозии обусловлено воздействием их на кинетику электрохимических реакций, лежащих в основе коррозионного процесса. Механизм защитного действия ингибиторов связан, в первую очередь, с их адсорбцией на границе раздела металл-среда. [59]
Страницы: 1 2 3 4