Кинетика - второе - порядок
Cтраница 1
Кинетика второго порядка наряду с отсутствием замедления хлорид-ионом показывает, что переходное состояние содержит целую молекулу хлора как при замещении, так и при присоединении. Возможность того, что определяющая скорость стадия состоит в атаке анионом хлора на комплекс [ олефин, С1 ], образующийся из реагентов предравновесно, неприложима к ароматическому замещению, так как нельзя предположить никакой удовлетворительной функции для хлорид-иона. Такая кинетика кажется невероятной и для присоединения к олефинам, так как свойства хлорзамещенных ионов карбония, образующихся в этих реакциях присоединения, таковы, что они обычно не образуются в равновесных состояниях. В рамках этой гипотезы было бы трудно также объяснить роль хлорид-ионов в дальнейшем катализе реакции. [1]
Кинетика второго порядка, согласно приведенной выше схеме, наблюдалась также в некоторых других реакциях СО-группы, катализируемых гидроксил-ионом; при этом присоединение НО-иона происходит, несомненно, в стадии, определяющей скорость реакции. Однако кинетика других реакций присоединения к карбонильной группе значительно осложнена, ввиду того что нуклеофильные реагенты являются, вообще говоря, основаниями и СО-группа может фиксировать протоны, то, с одной стороны, кислоты уничтожают нуклеофильное действие реагента, а с другой стороны, они связываются с кислородом СО-группы, увеличивая ее электрофильную активность. Следовательно, в некоторых реакционных условиях кислоты обладают ускоряющим, а в других - замедляющим эффектом. Однако ряд качественных аргументов кажется вполне убедительным. [2]
Кинетика второго порядка, согласно приведенной выше схеме, наблюдалась также в некоторых других реакциях СО-группы, катализируемых гидроксил - ионом; при этом присоединение НО-иона происходит, несомненно, в стадии, определяющей скорость реакции. Однако кинетика других реакций присоединения к карбонильной группе значительно осложнена; ввиду того что нуклеофильные реагенты являются, вообще говоря, основаниями и СО-группа может фиксировать протоны, то, с одной стороны, кислоты уничтожают нуклеофильное действие реагента, а с другой стороны, они связываются с кислородом СО-группы, увеличивая ее электрофильную активность. Следовательно, в некоторых реакционных условиях кислоты обладают ускоряющим, а в других - замедляющим эффектом. Однако ряд качественных аргументов кажется вполне убедительным. [3]
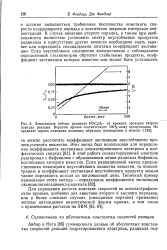
В случае кинетики второго порядка, а также при необходимости полностью установить спектр неустойчивых продуктов радиолиза в присутствии других веществ необходимо знать заранее или определить специальными опытами коэффициент экстинк-ции. [5]
Таким образом, кинетика второго порядка сводится к кинетике первого порядка. [6]
Прежде чем интерпретировать кинетику второго порядка, найденную Брауном и Инголдом ( Brown, Ingold, 1953) Для замещения в ионе [ Co ( H2NCH2CH2NH2) 2Cl2J ( например, на ион Njf), рассмотрим более общий вопрос о вероятном переходном состоянии при бимолекулярных реакциях, протекающих у окта-эдрических атомов. Если имеется указание на бимолекулярный механизм замещения у щестиковалентного атома металла, то часто постулируют промежуточное образование семиковалент-ного иона в качестве переходного состояния. О природе этого переходного состояния, делались различные предположения, но экспериментальные данные по этому вопросу еще недостаточны. [7]
Процесс вначале подчиняется кинетике второго порядка, которая к концу перехода отклоняется в сторону первого порядка. Это подтверждает ту точку зрения, что инициирование комплекса поли ( А У) сопряжено с образованием нескольких пар оснований, скрепленных водородными связями, за которым следует рост упорядоченных спиральных областей. При слиянии равных объемов эквимолекулярных растворов индивидуальных полирибонуклеотидов начальная скорость спирализа-ции пропорциональна квадрату концентрации однотяжевых макромолекул. [8]
Он приводит к кинетике второго порядка, так как, хотя замещающий агент Y - появляется в нем дважды, второе появление происходит после стадии, определяющей скорость. [9]
Для таких реакций характерна кинетика второго порядка. Точная природа переходного состояния зависит от нескольких переменных. [10]
Докажите, что реакция следует кинетике второго порядка. [11]
Большинство до сих пор изученных активируемых нуклеофильных замещений проявляет кинетику второго порядка ( первого порядка - для каждого реагирующего вещества), и для их объяснения было предложено два механизма. Один из них - простой одностадийный процесс, другой включает две стадии: образование и разложение промежуточного соединения некоторой стабильности. Хотя состоялось много дискуссий об относительных достоинствах этих механизмов, было уделено мало внимания тщательному собиранию неопровержимых доказательств ( как было сделано для алифатического нуклеофильного замещения), и, как часто случается в кинетических исследованиях, слишком мало экспериментально определенных параметров доступно для описания всех возможных эффектов. [12]
Кинетические исследования ряда примеров обнаружили для реакции азосочетания хорошо выдерживаемую кинетику второго порядка. Это вполне понятно, так как депротоиирован-ная гндроксигруппа является более сильным донором электронов, чем нейтральный гидрокевльный заместитель. Реакционная способность ионов диазония зависит от присутствия в ароматическом кольце заместителей. Электроноакцепторные заместители повышают, а электроно-донорные группы понижают реакционную способность ионов диазония. [13]
Схема Линдемана позволяет не только объяснить переход кинетики первого в кинетику второго порядка с изменением давления, но дает и аналитическую зависимость константы скорости от давления. [14]
Реакция газообразного аммиака с диоксидом азота на начальной стадии следует кинетике второго порядка. [15]
Страницы: 1 2 3 4