Кинетика - второе - порядок
Cтраница 2
Таким образом, реакция происходит в одну стадию и характеризуется кинетикой второго порядка: первым по субстрату и первым по основанию. Как и в механизме 5к2, уходящая группа может быть положительно заряженной или нейтральной, а основание отрицательно заряженным или нейтральным. [16]
Присутствие амфотерного растворителя объясняет, таким образом, наблюдаемую на опыте кинетику второго порядка. [17]
Если в переходном состоянии присутствует основание, то реакция будет иметь кинетику второго порядка. Во всех таких случаях разрыв связей С - Н и С-X должен происходить одновременно. Относительная степень расщепления двух связей в переходном состоянии может меняться в большом интервале в зависимости от природы уходящей группы и легкости удаления водорода в виде протона. [18]
Схема Линдемана не только позволяет объяснить переход кинетики первого порядка в кинетику второго порядка с изменением давления, но и дает аналитическую зависимость константы скорости от давления. [19]
Присутствие амфотерного растворителя объясняет, таким образом, наблюдаемую на опыте кинетику второго порядка. [20]
Для того чтобы показать, что вторая схема также приводит к кинетике второго порядка, можно применить принцип стационарного состояния. [21]
Данные Дарти и Сэваджа [107] по окислению кокса на алшмосиликатнам катализаторе отвечают кинетике второго порядка по коксу, данные ряда других исследователей [105, 113, 115] - кинетике первого порядка. [22]
Уравнение ( 68) не соответствует ни кинетике первого порядка, ни кинетике второго порядка. Попытки представить кривую затухания РЛ в виде суммы нескольких экспонент следует рассматривать как одну из возможных форм аналитического выражения опытной кривой; отдельные экспоненты не представляют различные физические процессы. [23]
На первый взгляд все эти процессы должны быть яркими примерами бимолекулярных реакций, подчиняющихся кинетике второго порядка. Однако реакции взаимодействия радикалов являются обратными по отношению к реакциям мономолекулярной диссоциации и поэтому они должны иметь и что-то общее. Это следует уже из того, что при всех давлениях должна сохраняться константа равновесия. [24]
Зная, что образование этого газа не подчиняется ни кинетике первого порядка, ни кинетике второго порядка, объясните, каким путем мог бы образоваться побочный продукт. [25]
Такая последовательность стадий согласуется с тем, что наблюдаемая реакция между S и Т подчиняется кинетике второго порядка. Образующийся амидат был идентифицирован проведением встречного синтеза и по ИК - и ЯМР-спектрам. [26]
Отщепление протона и уходящей группы или двух других групп происходит в одну стадию одновременно и характеризуется кинетикой второго порядка: первым по субстрату и первым по основанию, аналогичным для реакции 5д2 - замещения. По существу, обе реакции: Е2 и SV2 конкурируют друг с другом. Различие между двумя этими процессами заключается в направлении атаки реагента: частица с неподелениой парой электронов атакует атом углерода и действует как нуклеофил в 2-реакции, либо она атакует водород и действует как основание Бренстеда в Е2 - процессе. [27]
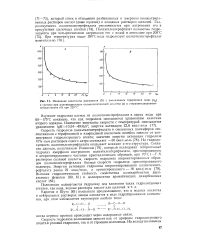 |
Изменение константы равновесия ( Л с увеличением содержания воды ( лш в системе при поликонденсации ш-аминогептановой кислоты ( а и гексаметилендиаммо-нийадипината ( б при 220 С. [28] |
Изучение гидролиза пленок из полиэтилентерефталата в парах воды при 60 - 175 С показало, что ход гидролиза описывается уравнением кинетики второго порядка. [29]
Как видим, все три значения k достаточно близки друг к другу; это подтверждает, что данная реакция имеет кинетику второго порядка. [30]
Страницы: 1 2 3 4