Кинетика - дегидратация
Cтраница 1
Кинетика дегидратации, спиртов в присутствии трехзамещенного фосфата кальция / / Изв. [1]
Кинетика дегидратации спиртов изучена рядом авторов. [2]
Кинетика дегидратации спиртов на сульфокатиони-тах также зависит от строения их каркаса. [3]
Кинетика дегидратации изопропилового спирта не может найти объяснение с точки зрения электронных свойств катализатора, подобно тому, как это сделано для дегидрогенизации циклогексана. [4]
Изучена кинетика дегидратации в области первого эндоэффекта. Это подтверждает предположение о том, что причиной спекания является образование полифосфатов уже на ранней стадии дегидратации. [5]
Изучена кинетика дегидратации изопропилового спирта и гидратации пропилена на пленочном фосфорнокислотном катализаторе в интервале температур 90 - 140 при суммарном давлении реагентов не выше атмосферного. [6]
Изучена кинетика дегидратации абсолютного этилового спирта на окиси алюминия, прокаленной при различных температурах. [7]
Исследование кинетики дегидратации трет. [8]
Изучение кинетики дегидратации этилового спирта с целью определения величин адсорбционного коэффициента воды производилось при температурах 415 и 450 как в присутствии продукта реакции - воды, так и с добавками инертного газа - аргона. [9]
Показано, что кинетика дегидратации этилового спирта в присутствии воды и аргона вполне удовлетворительно описывается уравнениями, в основу которых положена изотерма Лэнгмюра. [10]
В результате исследования кинетики дегидратации этилового спирта в зависимости от температуры как с добавлением к исходной смеси воды, так и аргона оказалось, что величина J5 остается равной единице во всех без исключения случаях. Равенство величины р единице соответствует предельному случаю, когда сумма адсорбционных коэффициентов продуктов реакции намного больше всех других величин, определяющих величину [ 3, в том числе и значения адсорбционного коэффициента реагирующего вещества, так как только при этом условии значение величины Р может быть равно единице. [11]
Борк и А. А. Толстопятовой изучена кинетика дегидратации спиртов и показано, что молекула спирта при дегидратации адсорбируется на поверхности катализатора группой СН-СОН. [12]
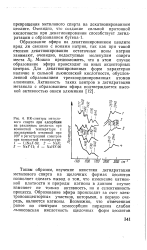
Результаты опытов по изучению кинетики дегидратации этилового спирта на черенковой окиси алюминия, а также на А12О3, обработанной фтористым бором, приводятся на рис, 1, из которого видно, что адсорбция фтористого бора увеличивает активность АЬОз во всем измеренном интервале объемных скоростей. При изучении кинетики было замечено, что активность катализатора, содержащего фтористый бор, не остается постоянной, а постепенно снижается на 1 - 2 % от опыта к опыту и при пропускании спирта с одной и той же объемной скоростью степень превращения его в этилен совпадает с уэт для чистой окиси алюминия. Изменение активности в данном случае, по-видимому, связано с последовательным удалением адсорбированного фтористого бора с поверхности окиси алюминия спиртом или продуктами его разложения. [13]
Таким образом, изучение кинетики дегидратации метилового спирта на щелочных формах цеолитов позволяет сделать вывод о том, что изменение катион-ной плотности и природы катиона в данном случае изменяет не только активность, но и селективность процесса. Образование эфира происходит за счет элек-троноакцепторных участков, которыми, в первую очередь, являются катионы. [15]
Страницы: 1 2 3