Классическая кинетика
Cтраница 3
Классическая кинетика, основываясь на законе действующих масс и на законе распределения Максвелла - Больцма-на, создала фундаментальные - количественные зависимости скорости протекания химических реакций от таких основных параметров, как концентрация реагирующих веществ, температура и давление процесса. [31]
Как мы уже говорили, гипотеза о том, что при реакции достигается адсорбционное равновесие по отношению к молекулам всех сортов, совершенно необоснованна. Тем не менее классическая кинетика, которая основана на применении изотермы Ленгмюра, позволила объяснить целый ряд экспериментальных данных. [32]
Фаулер сказал мне, что первый том моей книги выйдет очень скоро ( через несколько месяцев), в то время как второй сейчас пошел в печать. Второй том будет посвящен классической кинетике и квантовой теории как равновесия, так и кинетики. [33]
В рассмотренных простейших примерах видны некоторые существенные особенности электронной кинетики. Они сводятся к возможности имитации классической кинетики и кинетики на неоднородных поверхностях, к эффектам активирования и торможения, к влиянию па процесс различных факторов, вызывающих генерацию или разрушение дефектов. Характерны антагонистические действия добавок доноров и акцепторов-и можно ожидать компенсационных эффектов при введении смесей добавок и противоположного поведения п - и р-полупроводников. Любопытно, что в этом приближении для полупроводников с собственной проводимостью можно ожидать сходных эффектов, так как хотя электропроводность их растет как при добавлении акцепторных, так и при добавлении донорпых примесей, но, поскольку переходный комплекс имеет определенный знак, рост электропроводности будет в одном случае сопровождаться ростом активности, а в другом - его падением. [34]
Вероятность того, что в системе сталкивающихся частиц произойдет химическая реакция, определяется, в частности, наличием запаса энергии, необходимого для преодоления потенциального барьера. Учет этой вероятности в рамках классической кинетики проводят, например, на основе следующего допущения. Предполагают, что вероятность реакции равна нулю, если энергия системы сталкивающихся частиц меньше энергии U, соответствующей вершине потенциального барьера. Если же энергия, указанной системы больше или равна U, то вероятность реакции равна единице или постоянной величине, отличной от нуля. [35]
В большинстве случаев теория абсолютных скоростей лишь уточняет выводы классической кинетики, основанной на изотермах Ленгмюра. Поэтому все возражения, выдвигавшиеся против классической кинетики, сохраняются и здесь. [36]
Наметилась возможность неожиданного синтеза таких, казалось бы, далеких областей науки, как химическая кинетика, с одной стороны, и теория теплопередачи, диффузии, гидродинамика - с другой. Процессы, которые раньше считались в классической кинетике возмущениями, искажающими ход химической реакции, приобрели особый интерес именно в комбинации с химическим процессом. [37]
Как было сказано выше, на кривой зависимости числа частиц от конверсии на участке постоянной скорости полимеризации этил-акрилата существует максимум, причем после исчезновения капель мономера скорость все еще остается постоянной. Таким образом, наблюдаются существенные отклонения от классической кинетики, предполагающей постоянство числа частиц и концентрации в них мономера на стационарном участке. [38]
Мы рассмотрим лишь общие основы этой сложной проблемы, которая до сих пор еще не получила достаточно удовлетворительного количественного разрешения. Подходить к ней можно как с точки зрения классической кинетики, выражаемой уравнением ( 6 - 7), так и основываясь на рассматриваемом ниже методе переходного состояния, который раскрывает физический смысл множителя Р и дает более полное решение задачи. [39]
Кроме того, изучение скорости топохимических реакций, как правило, проводится либо по изменению массы твердого вещества, либо по количеству выделившегося газа. Поэтому исследователь не располагает таким параметром, характерным для классической кинетики, как концентрация реагирующего вещества. Эти специфические особенности не позволяют применять к топохимическим реакциям описанные ранее методы составления уравнений кинетики, исходя из совокупности элементарных химических реакций ( стадий) протекания процесса разложения твердых веществ. [40]
Все катализаторы крекинга подвержены деактивации, происходящей тем быстрее, чем выше активность катализатора. Потеря активности сопровождается превращениями, которые не рассматриваются в классической кинетике и катализе. Эти превращения хорошо описываются теорией ВПП; с ее помощью удалось объяснить особенности каталитического крекинга, за исключением различий в селективности, при использовании экспериментальных реакторов с неподвижным слоем катализатора и промышленных аппаратов с движущимся или псевдоожижепным слоем. Теория ВПП позволяет установить схему первичных реакций при крекинге индивидуальных углеводородов, а также оценить поведение свежего незакоксованного катализатора в начальной стадии процесса. Это открывает возможность для1 изучения природы активных центров кинетическими методами. [41]
В заключение следует отметить, что все реакции горения газа цепные с разветвленными цепями. В связи с этим суммарные реакции горения не подчиняются законам классической кинетики - закону действующих масс и закону Аррениуса. Однако эти законы остаются справедливыми при применении их к промежуточным реакциям суммарного процесса горения. [42]
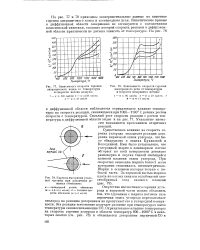 |
Зависимость скорости горения антрацитового кокса от температуры.| Зависимость скорости горения.| Картина выгорания угольной частицы при различных режимах обтекания. [43] |
На рис. 77 и 78 приведены экспериментальные данные по кинетике горения антрацитового кокса и электродного угля. Кинетические кривые в диффузионной области совершенно не согласуются с положениями классической кинетики, согласно которой скорость реакции в диффузионной области практически не должна зависеть от температуры. [44]
Применительно к реакциям, протекающим в растворах, теория кислотно-основного катализа дает достаточно надежные количественные кинетические характеристики специфического характера. Наряду с этим теория допускает количественное описание кислотно-основных реакций на основе как классической кинетики, так и новейших кинетических теорий - активного комплекса, цепной, мультиплетной. В этом смысле теория кислотно-основного катализа дополняет последние сведениями об особенностях кислотно-основного, или донорно-акцеп-торного взаимодействия, а другие теории дополняют ее своими данными. [45]
Страницы: 1 2 3 4