Общая кинетика
Cтраница 1
Общая кинетика таких реакций, очевидно, чрезвычайно сложна. [1]
Общая кинетика реакции определяется во многих случаях скоростями диффузии реагента. Это может быть установлено путем измерения температурной зависимости реакции. Если энергия активации равна нескольким килокалориям на моль, ход реакции обусловлен диффузионными процессами, поскольку энергия активации большинства химических реакпий составляет не единицы, а десятки килокалорий на моль. [2]
Общая кинетика биологических явлений определяется наиболее медленным их этапом - диффузией реагентов, а не биохимическими реакциями, протекающими при участии ферментов с очень большой скоростью. [3]
Некоторые положения общей кинетики, рассмотренные в первом издании, здесь опущены, что обусловлено ограничением объема монографии; предполагается, что читатель имеет необходимую элементарную подготовку. [4]
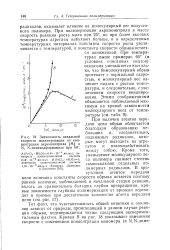 |
Зависимость начальной скорости полимеризации от концентрации акрилонитрила [ М ] в N, N-диметилформамиде при 60Э. [5] |
Тот факт, что чувствительность общей кинетики к окклюзии зависит от природы, происходящей в данном случае реакции обрыва, подтверждается также следующим экспериментальным фактом. [6]
Рассмотрим далее зависимость между молекулярно-стью и общей кинетикой реакции. Если бы можно было установить механизм реакции независимо от экспериментального уравнения скорости реакции, тогда бы уравнение скорости следовало из механизма. Например, если реакция действительно проходит в одну стадию и является бимолекулярной, то в экспериментальном уравнении скорости появилось бы два сомножителя, обозначающих концентрации, и это была бы реакция второго порядка. Но на практике предложенный механизм реакции требует экспериментального подтверждения, как и все другие теории, а доказательство всегда привлекает экспериментальное уравнение скорости реакции. Поэтому выводить уравнение скорости реакции из механизма - все равно, что кружить на одном месте. [7]
 |
Общая кинетика процесса.| Влияние хлористого водорода. [8] |
Для исследования явления рекомендуется разделить переменные за счет вырождения общей кинетики. [9]
Даже следы примесей в растворе, в основном органических, могут влиять на общую кинетику. Разногласия, которые существуют в литературе относительно реакции ( двух - или четырехэлектронные процессы На платине при ионизации кислорода, казалось бы, в одних и тех же экспериментальных условиях), по крайней мере частично, обусловлены разной степенью загрязнений. [10]
Процесс гидролиза для синтетического продукта протекает по законам мономолекулярных реакций и, повидимому, этой стадией определяется общая кинетика всей реакции. Тот же характер кинетики установлен нами и для реакции взаимодействия углекислых солей магния и двухвалентного железа с растворами хлористого кальция. Напротив, углекислый кальций не подвергается процессам гидролиза и не образует гидрооксикарбонатов. В этом, повидимому, лежит причина, по которой рассматриваемая реакция, по существу, необратима, так как скорость взаимодействия углекислого кальция с раствором хлорида марганца весьма мала. В термодинамическом же смысле она обратима, так как достигаются равновесные состояния, определяемые одинаковыми концентрациями ионов СО8 - или НСО8 - для обоих карбонатов. [11]
В последние годы нами проделана большая работа, назначение которой можно охарактеризовать как попытку сближения теории электрохимической кинетики с опытом общей кинетики химических реакций. [12]
Кривая такого типа характерна для реакции ( 1) - е - ( 2) или, точнее, она характеризует общую кинетику этой реакции, поскольку плотность тока пропорциональна скорости, с которой Происходит обмен электронов на границе фаз металл - раствор. Общая скорость процесса определяется скоростями массопере-носа и переноса заряда; оба эти явления всегда наблюдаются в электрохимических процессах. [13]
Под воздействием жидких сред, во-видимому, могут реализоваться все три механизма, что сильно затрудняет оценку вклада каждого из них в общую кинетику биодеградации и прогнозирование поведения полимера в организме на основе исследований в модельных условиях. Особенно это относится к изучению третьего механизма, который практически может быть косвенно оценен лишь на основании эксперимента на живом организме. [14]
Например, если внешнее сопротивление достаточно велико и, следовательно, определяет скорость разложения амальгамы, то изменение остальных условий процесса будет мало сказываться на общей кинетике реакции. Поэтому экспериментальные данные о зависимости силы тока короткого замыкания элемента от различных факторов соответствует лишь данной модели разлагателя. [15]
Страницы: 1 2 3