Электрохимическая кинетика
Cтраница 2
Закономерности электрохимической кинетики имеют существенное значение для истолкования механизма взаимодействия между металлами и растворами электролитов, лежащего в основе большей части коррозионных явлений. [16]
Раздел электрохимической кинетики, задачей которого является изучение стадий подвода реагирующих частиц к поверхности электрода и отвода продуктов реакции, называют электрохимической макрокинетикой или диффузионной кинетикой. [17]
Изучение электрохимической кинетики, этого важнейшего раздела электрохимии, способствует выяснению механизма и регулированию, совершенствованию и интенсификации разнообразнейших электродных процессов в электролизерах и при использовании химических источников электрической энергии. [18]
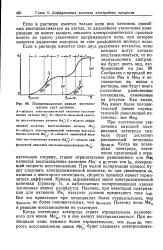 |
Поляризационная кривая восстановления двух катионов. [19] |
А-область электрохимической кинетики восстановления катиона Me; В - область смешанное кинетики восстановления катиона Me; С-область днффу. [20]
Рассмотрим электрохимическую кинетику для случая, когда собственно электрохимическая реакция является лимитирующей стадией и практически полностью определяет скорость процесса в целом. Это может быть, например, кинетика электроосаждения меди на медный электрод, погруженный в раствор, содержащий ионы меди. [21]
В электрохимической кинетике оперируют не с опытно неопределяемыми гальвани-потенциалами, а с электродными потенциалами Е, измеряемыми по отношению к определенному электроду сравнения Мй. В частности, сравнивают скорости электрохимических реакций на разных электродах при одном ц том же значении электродного потенциала, а не при одном и том же значении гальвани-потенциала Заменяя в уравнении (14.23) Фв м - 3 на Е цум. [22]
В электрохимической кинетике большое внимание уделяется изучению процесса передачи электронов, так как эта стадия является определяющей характер зависимости ток - потенциал. [23]
В электрохимической кинетике используются также понятия быстрые и медленные электродные реакции. Они являются весьма относительными и характеризуют скорость электродной реакции в масштабе времени наблюдения. Так, реакция считается быстрой, если ее скорость заметно превосходит скорость отклика прибора или его разрешающую способность во времени. Однако реакция, считающаяся быстрой при ее изучении одним методом, может оказаться медленной при использовании другого метода. Существует и другой подход. [24]
В электрохимической кинетике описание электродных про-цессо в неразрывно связано с представлениями о строении двойного электрического слоя. Течение реакции на электроде, например, сопровождается прохождением заряженной частицы ( иона или электрона) через двойной электрический слой либо из объема раствора к электроду, либо в обратном направлении. [25]
В электрохимической кинетике измеряют скорости суммарного процесса и составляющих его стадий в зависимости от заданной плотности тока. От других кинетических исследований кинетика электродных процессов отличается возможностью регулирования высот барьеров свободной энергии процессов гетерогенного переноса заряда с помощью изменения падения напряжения на фазовой границе. Перед изучением электрохимической кинетики желательно иметь термодинамическое описание системы; выявляют все реагенты, продукты промежуточных соединений, определяют стехиометрию полного процесса. [26]
Согласно закону электрохимической кинетики скорость анодного растворения должна возрастать при увеличении химического потенциала, однако в рассматриваемом случае этого не происходит. Вследствие образования сервовитной пленки меди между анодными и катодными участками поверхности бронзы процесс растворения может полностью прекратиться, и тогда наступит установившийся режим трения. [27]
Важнейшей задачей электрохимической кинетики является установление природы и кинетических параметров промежуточных стадий, а также установление взаимосвязей кинетических параметров отдельных стадий и общей реакции. [28]
Согласно теории электрохимической кинетики в тонких слоях нейтральных электролитов, развитой И. Л. Розенфельдом [294], процесс восстановления кислорода в пленках должен протекать с большей скоростью, чем в объеме раствора. А это значит, что металл, находящийся под пленкой электролита, всегда будет выступать в роли эффективного катода по отношению к участкам металла, расположенным в объеме электролита. На рис. 6.4 представлена схема трехфазной границы металл - электролит - нефтепродукт. [30]
Страницы: 1 2 3 4